题目内容
12.在下列自然资源的开发利用中,不涉及化学变化的是( )| A. | 用铁矿石冶炼铁 | B. | 用食醋清除暖水瓶中的水垢 | ||
| C. | 用煤生产水煤气 | D. | 干冰放在通风处自然升华 |
分析 A.铁矿石冶炼铁有新物质铁生成;
B.食醋能与碳酸钙反应,有新物质醋酸钙和二氧化碳生成;
C.煤生产水煤气有一氧化碳和氢气生成;
D.干冰放在通风处自然升华没有新物质生成.
解答 解:A.用铁矿石冶炼铁有新物质铁生成,涉及化学变化,故A错误;
B.食醋能与碳酸钙反应,有新物质醋酸钙和二氧化碳生成,故B错误;
C.用煤生产水煤气有一氧化碳和氢气生成,涉及化学变化,故C错误;
D.干冰放在通风处自然升华没有新物质生成,不涉及化学变化,故D正确.
故选D.
点评 本题考查物理变化与化学变化的判断,难度不大,要注意化学变化和物理变化的本质区别是否有新物质生成.

练习册系列答案
相关题目
3.${\;}_{19}^{40}$K、${\;}_{20}^{40}$Ca两种原子,它们具有相同的( )
| A. | 质子数 | B. | 中子数 | C. | 质量数 | D. | 电子数 |
20.下列说法正确的是( )
| A. | 在海轮船壳上镶入锌块保护海轮,利用的是牺牲阳极的阴极保护法 | |
| B. | 加入合适的催化剂,能降低反应活化能,从而改变反应的焓变 | |
| C. | 用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗醋酸的体积更大 | |
| D. | 稀醋酸中加入少量CH3COONa固体,醋酸的电离程度减小,c(CH3COO-)增大 |
17.下列实验方法正确的是( )
| A. | 用洁净的铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色,则溶液中一定不含有K+ | |
| B. | 配制一定物质的量浓度的溶液时,若加水超过容量瓶的刻度线,用胶头滴管将多余液体吸出即可 | |
| C. | 用过量的NaOH溶液鉴别AlCl3溶液和MgCl2溶液 | |
| D. | 检验某溶液中是否含有Fe2+时,可先加入适量的氯水,再滴加硫氰化钾溶液,若溶液变为红色,则说明溶液中一定含有Fe2+ |
4.对下列流程有关判断正确的是( )
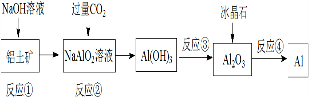

| A. | 流程中涉及的反应均为非氧化还原反应 | |
| B. | 反应②产生的阴离子主要为HCO3- | |
| C. | 实验室中完成反应③应在蒸发皿中进行 | |
| D. | 反应④的条件是高温加热 |
1.五种不同元素X、Y、Z、D、E、F的信息如下:
请回答下列问题:
(1)Z在周期表中的位置第三周期第ⅥA族,D的最高价氧化物对应水化物的电子式为
(2)X单质与D单质反应生成的D2X2能和H2O反应,写出其离子方程式为2Na2O2+2H2O═4Na++4OH-+O2↑.
(3)E元素与Y元素可形成EY2和EY3两种化合物,向淀粉碘化钾溶液滴加几滴EY3的浓溶液,原无色溶液可变为紫色,其原因是2Fe3++2I-═2Fe2++I2(用离子方程式表示).
(4)E单质在发生吸氧腐蚀时的正极反应方程式O2+2H2O+4e-═4OH-
(5)F的一种复盐常用作净水剂,用离子方程式表示其净水原理Al3++3H2O═Al(OH)3(胶体)+3H+.
| 元素 | 有关信息 |
| X | 元素主要常见化合价为-2和-1价,原子半径为0.074nm. |
| Y | 所在主族序数与所在周期序数之差为4. |
| Z | 原子半径为0.102nm,核外最外层电子数是其电子层数的2倍,其气态氢化物与Y单质发生反应生成淡黄色固体. |
| D | 最高价氧化物对应的水化物,能电离出离子数、电子数都相等的阴、阳离子. |
| E | 单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏. |
| F | 元素所在的主族序数等于周期序数. |
(1)Z在周期表中的位置第三周期第ⅥA族,D的最高价氧化物对应水化物的电子式为

(2)X单质与D单质反应生成的D2X2能和H2O反应,写出其离子方程式为2Na2O2+2H2O═4Na++4OH-+O2↑.
(3)E元素与Y元素可形成EY2和EY3两种化合物,向淀粉碘化钾溶液滴加几滴EY3的浓溶液,原无色溶液可变为紫色,其原因是2Fe3++2I-═2Fe2++I2(用离子方程式表示).
(4)E单质在发生吸氧腐蚀时的正极反应方程式O2+2H2O+4e-═4OH-
(5)F的一种复盐常用作净水剂,用离子方程式表示其净水原理Al3++3H2O═Al(OH)3(胶体)+3H+.