题目内容
【题目】已知:用Pt﹣Rh合金催化氧化NH3制NO,其反应的微观模型及含氮生成物产率随反应温度的变化曲线分别如图①、图②所示:下列说法中,不正确的是( ) 
A.400℃时,生成的产物有N2、NO、H2O
B.800℃时,反应的化学方程式是:4NH3+5O2 ![]() ?4NO+6H2O
?4NO+6H2O
C.400℃﹣800℃间,Pt﹣Rh合金对N2的吸附力逐渐减弱
D.800℃以上,发生了反应:2NO(g)?O2(g)+N2(g)△H>0
【答案】C
【解析】解:A.根据图2知,400℃时,生成的含有N元素的产物有N2、NO且N2产率大于NO,同时产物中还有水,故A正确; B.800℃时,生成的含有N元素的产物主要是NO,接近100%,所以发生的反应为4NH3+5O2 ![]() 4NO+6H2O,故B正确;
4NO+6H2O,故B正确;
C.400℃﹣800℃间,N2的产率下降、NO产率上升,且NO产率接近100%,所以Pt﹣Rh合金对N2的吸附力增强而不是减弱,故C错误;
D.800℃以上,N2的产率上升、NO的产率下降,说明发生了反应2NO(g)O2(g)+N2(g),升高温度氮气产率增加,说明该反应的正反应是吸热反应,△H>0,故D正确;
故选C.

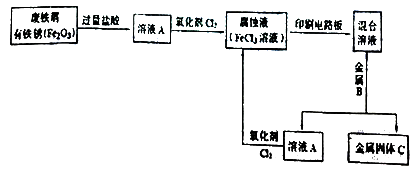
【题目】黄铁矿(主要成分FeS2)、黄铜矿(主要成分CuFeS2)均是自然界中的常见矿物资源. 
(1)黄铁矿在空气中易被氧化,其反应历程可能为如图1所示的四步: ①a反应中每生成1molFeSO4转移电子的物质的量为mol.
②d反应的离子方程式为 .
(2)用黄铜矿常温细菌冶铜和高温火法冶铜的流程如图2所示: ①细菌冶铜时,当黄铜矿中伴有黄铁矿可明显提高Cu2+的浸出速率,
其原理如图3所示:
Ⅰ.冶炼过程中,FeS2周边溶液的pH(填“增大”、“减小”或“不变”).
Ⅱ.从CuFeS2析出S的反应式是 .
②火法冶铜时,由Cu2S制得铜的化学方程式是 .
(3)煤炭中的硫主要以黄铁矿形式存在,用氢气脱除黄铁矿中硫的相关反应(见表),其相关反应的平衡常数与温度的关系如图4.
相关反应 | 反应热 | 平衡常数 |
FeS2(s)+H2(g)FeS(s)+H2S(g) | △H1 | K1 |
| △H2 | K2 |
FeS(s)+H2(g)Fe(s)+H2S(g) | △H3 | K3 |
①上述反应中,△H10(填“>”或“<”).
②提高硫的脱除率可采取的措施有(举1例).