题目内容
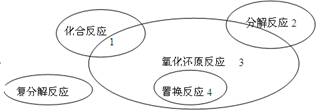
氧化还原反应与四种基本类型反应的关系如右图所示,则下列化学反应属于3 区域的是
A.Cl2+2KBr
Br2+2KCl
B.2NaHCO3 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
C.4Fe(OH)2+O2+2H2O
4Fe(OH)3
D.2Na2O2+2CO2
2Na2CO3+O2
【答案】
D
【解析】
试题分析:根据图示可以看出3区域的反应属于非化合、分解、置换反应的氧化还原反应。氧化还原反应必须有化合价的变化,化合反应是多种反应物变成一种生成物,分解反应是一种反应物变成多种生成物,置换反应必须有单质参加和单质生成,因此D符合。答案选D。
考点:化学反应类型
点评:本题主要根据反应的特点来进行判断,非常基础简单。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

 或HOCOOH
或HOCOOH
 (2011?江苏)原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物种最多的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.
(2011?江苏)原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物种最多的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.