题目内容
下列叙述正确的是
- A.将pH=2的盐酸和pH=2的醋酸等体积混合,混合后溶液的pH=2
- B.HA-比HB-更难电离,则NaHA溶液的pH一定比NaHB溶液的大
- C.在饱和氨水中加入同浓度的氨水,平衡正向移动
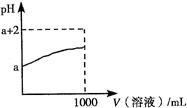
- D.某温度下,Ba(OH)2溶液中,Kw=10-12,pH=8的该溶液中加入等体积pH=4的盐酸,混合溶液的pH=7
A
试题分析:A、两种溶液等体积混合后醋酸分子和醋酸根的浓度都下降为原来的一半,但两者的比值不变,混合后氢离子浓度也不变,所以QC等于Ka,平衡不移动,混合后溶液的pH等于2,正确;B、若NaHA溶液和NaHB溶液都是碱性溶液,则需要考虑H2A和H2B的酸性才能确定溶液pH的关系,错误;C、平衡不移动,错误;D、恰好中和得到中性溶液,pH= 6,错误。
考点:考查电解质溶液、电离平衡、离子浓度计算知识。
试题分析:A、两种溶液等体积混合后醋酸分子和醋酸根的浓度都下降为原来的一半,但两者的比值不变,混合后氢离子浓度也不变,所以QC等于Ka,平衡不移动,混合后溶液的pH等于2,正确;B、若NaHA溶液和NaHB溶液都是碱性溶液,则需要考虑H2A和H2B的酸性才能确定溶液pH的关系,错误;C、平衡不移动,错误;D、恰好中和得到中性溶液,pH= 6,错误。
考点:考查电解质溶液、电离平衡、离子浓度计算知识。

练习册系列答案
相关题目
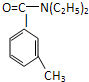 避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH
避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH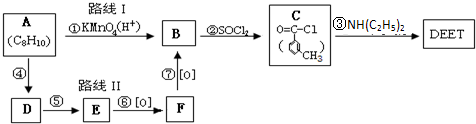


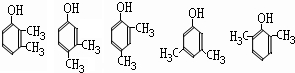 (任写2种)
(任写2种)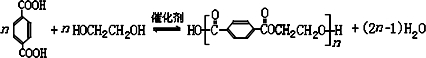

 NH3?H2O+H+
NH3?H2O+H+ (2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.
(2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.