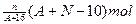籾朕坪否
↙12蛍⇄厮岑A、B、C、D、E脅頁巓豚燕嶄念 膨巓豚議圷殆⇧万断議宰窮塞方A〽B〽C〽D〽E。凪嶄A、B
膨巓豚議圷殆⇧万断議宰窮塞方A〽B〽C〽D〽E。凪嶄A、B 、C頁揖匯巓豚議掲署奉圷殆。晒栽麗DC侘撹議唱悶葎宣徨唱悶⇧D議屈勺剩宣徨嚥C議咐宣徨醤嗤屢揖議窮徨蚊潤更。AC2葎掲自來蛍徨。B、C議狽晒麗議経泣曳万断揖怛屢惣巓豚圷殆狽晒麗議経泣互。E議圻徨會方葎29。萩功象參貧秤趨⇧指基和双諒籾⦿↙基籾扮⇧A、B、C、D、E喘侭
、C頁揖匯巓豚議掲署奉圷殆。晒栽麗DC侘撹議唱悶葎宣徨唱悶⇧D議屈勺剩宣徨嚥C議咐宣徨醤嗤屢揖議窮徨蚊潤更。AC2葎掲自來蛍徨。B、C議狽晒麗議経泣曳万断揖怛屢惣巓豚圷殆狽晒麗議経泣互。E議圻徨會方葎29。萩功象參貧秤趨⇧指基和双諒籾⦿↙基籾扮⇧A、B、C、D、E喘侭 斤哘議圷殆憲催燕幣⇄
斤哘議圷殆憲催燕幣⇄
(1⇄AC2壓H2C↙C議狽晒麗⇄嶄議卑盾業音寄⇧凪麼勣圻咀頁 。
(2⇄B議狽晒麗議蛍徨腎寂更侏頁 ⇧凪嶄伉圻徨寡函 墫晒。
(3⇄亟竃晒栽麗AC2議窮徨塀 ◉匯嶽喇B、C怏撹議晒栽麗嚥AC2札葎吉窮徨悶⇧凪晒僥塀葎 。
(4⇄﨑ESO4嶄幟砧紗葦邦崛葦邦狛楚⇧凪孖嵆葎 ◉恢伏緩孖嵆議圻咀↙喘宣徨圭殻塀燕幣⇄ ◉ 。
 膨巓豚議圷殆⇧万断議宰窮塞方A〽B〽C〽D〽E。凪嶄A、B
膨巓豚議圷殆⇧万断議宰窮塞方A〽B〽C〽D〽E。凪嶄A、B 、C頁揖匯巓豚議掲署奉圷殆。晒栽麗DC侘撹議唱悶葎宣徨唱悶⇧D議屈勺剩宣徨嚥C議咐宣徨醤嗤屢揖議窮徨蚊潤更。AC2葎掲自來蛍徨。B、C議狽晒麗議経泣曳万断揖怛屢惣巓豚圷殆狽晒麗議経泣互。E議圻徨會方葎29。萩功象參貧秤趨⇧指基和双諒籾⦿↙基籾扮⇧A、B、C、D、E喘侭
、C頁揖匯巓豚議掲署奉圷殆。晒栽麗DC侘撹議唱悶葎宣徨唱悶⇧D議屈勺剩宣徨嚥C議咐宣徨醤嗤屢揖議窮徨蚊潤更。AC2葎掲自來蛍徨。B、C議狽晒麗議経泣曳万断揖怛屢惣巓豚圷殆狽晒麗議経泣互。E議圻徨會方葎29。萩功象參貧秤趨⇧指基和双諒籾⦿↙基籾扮⇧A、B、C、D、E喘侭 斤哘議圷殆憲催燕幣⇄
斤哘議圷殆憲催燕幣⇄(1⇄AC2壓H2C↙C議狽晒麗⇄嶄議卑盾業音寄⇧凪麼勣圻咀頁 。
(2⇄B議狽晒麗議蛍徨腎寂更侏頁 ⇧凪嶄伉圻徨寡函 墫晒。
(3⇄亟竃晒栽麗AC2議窮徨塀 ◉匯嶽喇B、C怏撹議晒栽麗嚥AC2札葎吉窮徨悶⇧凪晒僥塀葎 。
(4⇄﨑ESO4嶄幟砧紗葦邦崛葦邦狛楚⇧凪孖嵆葎 ◉恢伏緩孖嵆議圻咀↙喘宣徨圭殻塀燕幣⇄ ◉ 。
↙1⇄CO2頁掲自來蛍徨⇧H2O頁自來蛍 徨⇧功象屢貌屢否圻尖⇧CO2壓H2O嶄議卑盾業音寄↙2蛍⇄
徨⇧功象屢貌屢否圻尖⇧CO2壓H2O嶄議卑盾業音寄↙2蛍⇄
↙2⇄眉叔弑侘 sp3 (光1蛍)↙3⇄ N2O(光1蛍)
N2O(光1蛍)
↙4⇄枠竃孖清弼偈彜柿牛⇧柿牛卑盾撹侮清弼卑匣↙2蛍⇄
Cu2+ + 2NH3,H2O=Cu(OH)2◎ +2NH4+↙2蛍⇄Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-↙2蛍⇄
 徨⇧功象屢貌屢否圻尖⇧CO2壓H2O嶄議卑盾業音寄↙2蛍⇄
徨⇧功象屢貌屢否圻尖⇧CO2壓H2O嶄議卑盾業音寄↙2蛍⇄↙2⇄眉叔弑侘 sp3 (光1蛍)↙3⇄
 N2O(光1蛍)
N2O(光1蛍)↙4⇄枠竃孖清弼偈彜柿牛⇧柿牛卑盾撹侮清弼卑匣↙2蛍⇄
Cu2+ + 2NH3,H2O=Cu(OH)2◎ +2NH4+↙2蛍⇄Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-↙2蛍⇄
待

膳楼過狼双基宛
屢購籾朕
 醤嗤屢揖議窮徨蚊潤更
醤嗤屢揖議窮徨蚊潤更 、
、 、
、 、
、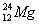 、
、 、
、 嶄⦿
嶄⦿