题目内容
在25℃时,将气体X、Y放入密闭容器中发生反应生成Z,5min后达到平衡.其初始浓度和平衡浓度如下表:
|
分析:A、依据图表中的初始浓度和平衡浓度判断反应物和生成物,依据变化的浓度计算反应比写出化学方程式;
B、根据化学平衡的变化量和转化率的概念列式计算;
C、依据化学反应速率的概念计算,单位时间内物质浓度的变化为物质表示的反应速率;
D、依据化学方程式反应前后的气体体积变化,结合平衡影响因素分析判断.
B、根据化学平衡的变化量和转化率的概念列式计算;
C、依据化学反应速率的概念计算,单位时间内物质浓度的变化为物质表示的反应速率;
D、依据化学方程式反应前后的气体体积变化,结合平衡影响因素分析判断.
解答:解:A、5min后达到平衡,X的消耗浓度为0.05mol/L;Y的消耗浓度为0.15mol/L;Z的生成浓度为0.1mol/L;反应物和生成物的物质的量之比为:1:3:2,化学方程式为:X+3Y=2Z,故A正确;
B、X的变化浓度为0.05mol/L,转化率=
×100%=50%,故B正确;
C、前5min 以Y表示的平均反应速率=
=0.03mol/L?min,故C错误;
D、反应正向是气体体积减小的反应,增大压强平衡向生成Z的方向进行,故D正确;
故选C.
B、X的变化浓度为0.05mol/L,转化率=
| 0.05mol/L |
| 0.1mol/L |
C、前5min 以Y表示的平均反应速率=
| 0.2mol/L-0.05mol/L |
| 5min |
D、反应正向是气体体积减小的反应,增大压强平衡向生成Z的方向进行,故D正确;
故选C.
点评:本题考查了化学平衡的有关计算,化学方程式的书写方法,化学反应速率的计算,反应物的质量的计算,影响化学平衡的因素分析判断,题目难度中等.

练习册系列答案
相关题目
在25℃时,将气体X、Y放入密闭容器中发生反应生成Z,5min后达到平衡。其初始浓度和平衡浓度如下表:下列说法错误的是 
A.该反应可表示为 X+3Y 2Z 2Z |
| B.反应达到平衡时,X的转化率为50% |
| C.前5min 以Y表示的平均反应速率为υ(Y)=" 0.01" mol·L-1·min-1 |
| D.增大压强使平衡向生成Z的方向移动 |
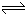 xC(g)+2D(g) ;△H>0,经5min后测知D的浓度为0.5mol/L,
xC(g)+2D(g) ;△H>0,经5min后测知D的浓度为0.5mol/L, xC(g)+2D(g)
;△H>0,经5min后测知D的浓度为0.5mol/L,
xC(g)+2D(g)
;△H>0,经5min后测知D的浓度为0.5mol/L,