题目内容
已知298K时反应2SO2( g ) + O2( g )  2SO3( g );△H =" -197" kJ · mol-1,在相同温度下向一密闭容器中加入2 mol SO2和1 molO2,达化学平衡时放出热量为a1 kJ ;向另一容积相同的密闭容器中通入 1 mol SO2和0.5 molO2,达化学平衡时放出热量为a2 kJ ,则下列关系式中正确的是( )
2SO3( g );△H =" -197" kJ · mol-1,在相同温度下向一密闭容器中加入2 mol SO2和1 molO2,达化学平衡时放出热量为a1 kJ ;向另一容积相同的密闭容器中通入 1 mol SO2和0.5 molO2,达化学平衡时放出热量为a2 kJ ,则下列关系式中正确的是( )
 2SO3( g );△H =" -197" kJ · mol-1,在相同温度下向一密闭容器中加入2 mol SO2和1 molO2,达化学平衡时放出热量为a1 kJ ;向另一容积相同的密闭容器中通入 1 mol SO2和0.5 molO2,达化学平衡时放出热量为a2 kJ ,则下列关系式中正确的是( )
2SO3( g );△H =" -197" kJ · mol-1,在相同温度下向一密闭容器中加入2 mol SO2和1 molO2,达化学平衡时放出热量为a1 kJ ;向另一容积相同的密闭容器中通入 1 mol SO2和0.5 molO2,达化学平衡时放出热量为a2 kJ ,则下列关系式中正确的是( )| A.2a2<a1< 197 |
| B.2a2>a1 >197 |
| C.2a2 = a1 >197 |
| D.2a2 = a1 = 197 |
A
题中热化学方程式中的热量表示生成2 mol SO3放出197 kJ热量,在一密闭容器中加入2 mol SO2和1 mol O2,由于反应是可逆反应,所以生成的SO3的物质的量总是小于2 mol,则放出的热量小于197 kJ,即a1 < 197;在另一个相同容积的容器中,注入的SO2和O2的物质的量减为一半,若容器容积也为原来的一半,则此化学平衡与原平衡等效,放出热量为a2 / 2,现将容积扩大到相同,则化学平衡向逆反应方向移动,所以放出的热量小于a1 / 2,即a1 > 2a2,所以选项A正确。

练习册系列答案
相关题目

 2C(g)+xD(g);ΔH<0,经5 min达平衡,此时生成2 mol C,测得D的平均反应速率为0.1 mol·(L·min)-1,下列说法正确的是
2C(g)+xD(g);ΔH<0,经5 min达平衡,此时生成2 mol C,测得D的平均反应速率为0.1 mol·(L·min)-1,下列说法正确的是 bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y和Z的浓度均是原来的1.8倍。则下列叙述正确的是
bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y和Z的浓度均是原来的1.8倍。则下列叙述正确的是  xC(g)有如下图(a)、(b)所示的关系曲线,试判断下列对图(b)的说法正确的是 ( )
xC(g)有如下图(a)、(b)所示的关系曲线,试判断下列对图(b)的说法正确的是 ( )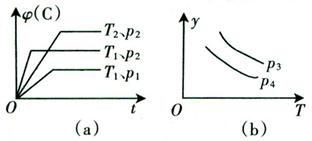
 bR(g)达到平衡后,温度和压强对该反应的影响如下图所示,图中压强p1> p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。据此可判断( )
bR(g)达到平衡后,温度和压强对该反应的影响如下图所示,图中压强p1> p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。据此可判断( ) 



 等于___________________________;
等于___________________________; 2NO(g)+O2(g)。将1molNO2、0.2molO2和一定量的NO通入容积为2L的密闭容器内反应,10min后反应恰好达到平衡状态,此时容器内有0.6molNO,容器内压强为原来的8/7。计算:(要求有计算过程)
2NO(g)+O2(g)。将1molNO2、0.2molO2和一定量的NO通入容积为2L的密闭容器内反应,10min后反应恰好达到平衡状态,此时容器内有0.6molNO,容器内压强为原来的8/7。计算:(要求有计算过程)