题目内容
某同学设计了以下流程来检验碳酸钠粉末中可能含有少量氯化钠和氢氧化钠中的一种或两种杂质.
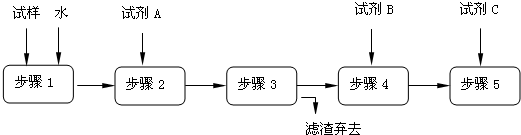
(1)步骤1所需玻璃仪器是______;步骤3的操作名称是______.
(2)对检验碳酸钠粉末中可能含有的杂质提出合理假设:
假设1:只含有氯化钠
假设2:只含有______
假设3:氯化钠和氢氧化钠都含有
(3)设计实验方案,进行试验.
限选以下试剂:氯化钡溶液、硝酸钡溶液、酚酞试液、稀硝酸、稀盐酸、稀硫酸、硝酸银溶液.回答下列问题:
①加入过量试剂A的名称是______.
②填写下表:

(1)步骤1所需玻璃仪器是______;步骤3的操作名称是______.
(2)对检验碳酸钠粉末中可能含有的杂质提出合理假设:
假设1:只含有氯化钠
假设2:只含有______
假设3:氯化钠和氢氧化钠都含有
(3)设计实验方案,进行试验.
限选以下试剂:氯化钡溶液、硝酸钡溶液、酚酞试液、稀硝酸、稀盐酸、稀硫酸、硝酸银溶液.回答下列问题:
①加入过量试剂A的名称是______.
②填写下表:
| 实验步骤 | 预期现象和结论 |
| 步骤4: | |
| 步骤5: |
(1)溶解固体使用的仪器有:盛放溶液的烧杯,加速固体溶解的仪器玻璃棒;分离固体和液体的方法是过滤.
故答案为:烧杯玻璃棒;过滤.
(2)假设2:只含有氢氧化钠
故答案为:氢氧化钠.
(3)①检验氯离子用硝酸银溶液,碳酸根离子和银离子反应也生成白色沉淀,所以会造成干扰,故应选取硝酸钡溶液先把碳酸根离子除去.
故答案为:硝酸钡溶液.
②步骤4:如果溶液中含有氢氧化钠,溶液就呈碱性,向溶液中滴加酚酞试液溶液会变成红色,如果不变成红色,就没有氢氧化钠.
步骤5:如果溶液中含有氯化钠,向溶液中滴加硝酸酸化的硝酸银溶液产生白色沉淀,就证明含有氯离子,否则没有氯离子,结合步骤4分析,如果溶液变红,假设3成立.
故答案为:
故答案为:烧杯玻璃棒;过滤.
(2)假设2:只含有氢氧化钠
故答案为:氢氧化钠.
(3)①检验氯离子用硝酸银溶液,碳酸根离子和银离子反应也生成白色沉淀,所以会造成干扰,故应选取硝酸钡溶液先把碳酸根离子除去.
故答案为:硝酸钡溶液.
②步骤4:如果溶液中含有氢氧化钠,溶液就呈碱性,向溶液中滴加酚酞试液溶液会变成红色,如果不变成红色,就没有氢氧化钠.
步骤5:如果溶液中含有氯化钠,向溶液中滴加硝酸酸化的硝酸银溶液产生白色沉淀,就证明含有氯离子,否则没有氯离子,结合步骤4分析,如果溶液变红,假设3成立.
故答案为:
| 实验步骤 | 预期现象和结论 |
| 步骤4: 取少量滤液于试管,往其中滴加2~3滴酚酞试液 | ①如果酚酞变红,假设2或假设3成立. ②如果酚酞不变红,假设1成立. |
| 步骤5: 用试管取少量滤液,往其中滴加足量的稀硝酸至溶液呈酸性,再滴加硝酸银溶液. | ①若没有白色沉淀生成,则说明假设2成立.②若有白色沉淀生成,则说明假设1或假设3成立;结合步骤4①如果酚酞变红,假设3成立 |

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目

 (1) 某学生用已知质量y克的表面皿,准确称取W克样品,他在托盘天平的右盘放入(W+y)克砝码,在左盘的表面皿中加入样品,这时指针偏向右边,如下图示。请补完整后面的操作是_______。
(1) 某学生用已知质量y克的表面皿,准确称取W克样品,他在托盘天平的右盘放入(W+y)克砝码,在左盘的表面皿中加入样品,这时指针偏向右边,如下图示。请补完整后面的操作是_______。