题目内容
7.设nA为阿伏加德罗常数的数值,下列说法正确的是( )| A. | 常温常压下,28g C2H4和C3H6的混合物中含有2nA个C原子 | |
| B. | 1 mol Fe与足量稀HNO3反应,转移个2nA个电子 | |
| C. | 1L 0.1 mol/L NaHCO3溶液中含有0.1nA个HCO3- | |
| D. | 常温常压下,22.4L的NO2和CO2混合气体含有2nA个O原子 |
分析 A.C2H4和C3H6的最简式为CH2,根据最简式进行计算;
B.稀硝酸足量,1mol铁完全反应生成1mol铁离子,转移了3mol电子;
C.碳酸氢根离子部分水解,导致溶液中碳酸氢根离子数目减少;
D.常温下不能使用标准状况下的气体摩尔体积计算.
解答 解:A.常温常压下,28g C2H4和C3H6的混合物中含有28gCH2,含CH2有的物质的量为$\frac{28g}{14g/mol}$=2mol,则混合物中含有2nA个C原子,故A正确;
B.1 mol Fe与足量稀HNO3反应生成1mol铁离子,失去3mol电子,转移了3nA个电子,故B错误;
C.1L 0.1 mol/L NaHCO3溶液中含有0.1mol碳酸氢钠,由于部分碳酸氢根离子部分水解,则溶液中含有的碳酸氢根离子的物质的量小于0.1mol,含有的碳酸氢根离子数目小于0.1nA,故C错误;
D.常温常压下,不能使用标准状况下气体摩尔体积计算22.4L的NO2和CO2混合气体的物质的量,故D错误;
故选A.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标准状况下气体摩尔体积的使用条件,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,试题有利于提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.下列实验操作能达到目的是( )
| A. | 用Na2S溶液和Al2(SO4)3溶液反应制取Al2S3固体 | |
| B. | 加热蒸发K2CO3溶液获得K2CO3晶体 | |
| C. | 加热蒸发FeCl2溶液制取Fe(OH)2固体 | |
| D. | 加热蒸发MgCl2溶液制取MgCl2固体 |
18.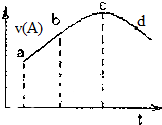 在恒温恒容的密闭容器中通入一定量的A、B,发生反应A(g)+2B(g)?3C(g)+D(l).如图是A的正反应速率v(A)随时间变化的示意图.下列说法正确的是( )
在恒温恒容的密闭容器中通入一定量的A、B,发生反应A(g)+2B(g)?3C(g)+D(l).如图是A的正反应速率v(A)随时间变化的示意图.下列说法正确的是( )
 在恒温恒容的密闭容器中通入一定量的A、B,发生反应A(g)+2B(g)?3C(g)+D(l).如图是A的正反应速率v(A)随时间变化的示意图.下列说法正确的是( )
在恒温恒容的密闭容器中通入一定量的A、B,发生反应A(g)+2B(g)?3C(g)+D(l).如图是A的正反应速率v(A)随时间变化的示意图.下列说法正确的是( )| A. | 反应物A的浓度:a点小于b点 | |
| B. | 可能是某种生物对反应起到的催化作用 | |
| C. | 曲线上的c、d两点都表示达到反应限度 | |
| D. | 平均反应速率:ab段大于bc段 |
15.下列过程中所发生的反应是取代反应的是( )
| A. | 光照甲烷和氯气的混合气体 | B. | 苯在镍催化作用下与氢气发生反应 | ||
| C. | 乙醇与酸性高锰酸钾溶液的反应 | D. | 苯和液溴混合加入铁粉的反应 |
2.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | pH=1的溶液中:K+、Fe2+、MnO${\;}_{4}^{-}$、SO${\;}_{4}^{2-}$ | |
| B. | c(Fe3+)=0.1 mol•L-1的溶液中:K+、ClO-、SO${\;}_{4}^{2-}$、SCN- | |
| C. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中:NH${\;}_{4}^{+}$、Al3+、NO${\;}_{3}^{-}$、Cl- | |
| D. | 与铝反应生成氢气的溶液中:NH${\;}_{4}^{+}$、K+、Cl-、SiO${\;}_{3}^{2-}$ |
19.下列物质在一定条件下可与CH4发生化学反应的是( )
| A. | 氢气 | B. | 溴水 | C. | 氧气 | D. | 酸性KMnO4溶液 |
17.0.1mol某有机物完全燃烧后生成0.3mol C02,同质量的该有机物与足量的金属钠反应生成0.1mol H2,该有机物可能是 ( )
| A. | 丙三醇 | B. | 1,2-丙二醇 | C. | 1,3-丙二醇 | D. | 乙二醇 |

 .
.