题目内容
测定一定质量的铝锌合金与强酸溶液反应产生的氢气的体积,可以求得合金中铝和锌的质量分数。现有下列实验用品:800 mL烧杯、100 mL量筒、短颈玻璃漏斗、铜网、铝锌合金样品、浓盐酸(密度1.19 g·mol-1)、水。按如图所示装置进行实验,完成下列问题(设合金样品完全反应,产生的气体体积不超过100 mL)。
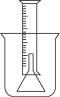
(1)补充下列实验步骤,直到反应开始进行(铁架台和铁夹的安装可省略):
①将称最后的合金样品用铜网小心包裹好,放在100 mL烧杯底部,把短颈漏斗倒扣在样品上面。
(2)合金样品用铜网包裹的目的是:_____________。

(1)补充下列实验步骤,直到反应开始进行(铁架台和铁夹的安装可省略):
①将称最后的合金样品用铜网小心包裹好,放在100 mL烧杯底部,把短颈漏斗倒扣在样品上面。
(2)合金样品用铜网包裹的目的是:_____________。
(1)②在烧杯中注入水,直到水面没过漏斗颈;③在100 mL量筒中装满水,倒置在盛水的烧杯中(量筒中不应留有气泡),使漏斗颈插入量筒中。烧杯中水面到杯口至少保留约100 mL空间。④将长颈漏斗(或玻璃棒)插入烧杯并接近烧杯底部,慢慢加入浓盐酸,至有气体产生。
(2)使样品在反应时能保持在烧杯底适当的位置(或答避免反应时样品漂浮)。
(2)使样品在反应时能保持在烧杯底适当的位置(或答避免反应时样品漂浮)。
在题目的第①步操作后,下一步只能是向烧杯中加入水,所加入的水必须浸没漏斗颈口,否则将无法继续操作。然后,将装满水的100 mL量筒倒置于盛水的烧杯中,至于怎样倒置,题目不作要求,但须注意漏斗颈一定要插入量筒内。
组装完成后可以开始反应,由于本题的合金样品全部反应产生的气体体积不会超过100 mL,因此,对加入的盐酸浓度和用量不作要求。
下一步应通过长颈漏斗加入浓盐酸,使用浓盐酸是为了加快反应速率。
由于金属是铝锌合金,密度较小,在跟盐酸反应时可以上下浮动,铝屑或铝片易顺着漏斗漂浮而出,给实验结果造成相当大的误差,所以用不与盐酸反应的铜网包裹,使之不致漂浮。
组装完成后可以开始反应,由于本题的合金样品全部反应产生的气体体积不会超过100 mL,因此,对加入的盐酸浓度和用量不作要求。
下一步应通过长颈漏斗加入浓盐酸,使用浓盐酸是为了加快反应速率。
由于金属是铝锌合金,密度较小,在跟盐酸反应时可以上下浮动,铝屑或铝片易顺着漏斗漂浮而出,给实验结果造成相当大的误差,所以用不与盐酸反应的铜网包裹,使之不致漂浮。

练习册系列答案
相关题目
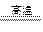 2MgO+Si(玻璃中含有一定量的二氧化硅),同时有副反应发生:2Mg+Si
2MgO+Si(玻璃中含有一定量的二氧化硅),同时有副反应发生:2Mg+Si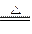 Mg2Si。Mg2Si遇盐酸迅速反应生成SiH4(硅烷)。SiH4在常温下是一种不稳定、易分解的气体。
Mg2Si。Mg2Si遇盐酸迅速反应生成SiH4(硅烷)。SiH4在常温下是一种不稳定、易分解的气体。
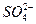 ====BaSO4↓
====BaSO4↓