题目内容
【题目】已知五种元素的原子序数的大小顺序为 C> A> B >D >E,A、C同周期,B、C同主族。A与B形成的离子化合物A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10电子的分子。试回答下列问题:
(1)写出以下元素的名称 A_________ C_________
(2)B元素在元素周期表中的位置是_______________;D2分子的结构式是______________。
(3)实验室制取D的氢化物的化学反应方程式为_________________________。
(4)用电子式表示化合物A2B的形成过程______________________。
(5)M、N均由A、B、C、E四种元素组成,写出此两种化合物在水溶液中发生反应的离子方程式____________________________。
【答案】 钠 硫 第二周期第ⅥA族 ![]() 2NH4Cl+Ca(OH)2
2NH4Cl+Ca(OH)2![]() CaCl2+ 2H2O+2NH3↑
CaCl2+ 2H2O+2NH3↑ ![]() H++HSO3-=SO2+H2O
H++HSO3-=SO2+H2O
【解析】A与B形成离子化合物A2B,A2B中所有离子的电子数相同,且电子总数为30,所以每个离子都有10个电子,由化学式的结构可知,B带2个单位负电荷,A带1个单位正电荷,所以A是Na元素,B是O元素,因为A、C同周期,B与C同主族,所以C为S元素;D和E可形成4核10电子的分子,每个原子平均不到3个电子,可知其中一定含有氢原子,分子中有4个原子核共10个电子,一定是NH3,结合原子序数D>E,可知D是N元素,E是H元素,则
(1)由上述分析可知,A为钠,C为硫;(2)氧元素位于第二周期第ⅥA族。氮气的结构式为![]() 。(3)实验室制备氨气的方程式为2NH4Cl+Ca(OH)2
。(3)实验室制备氨气的方程式为2NH4Cl+Ca(OH)2![]() CaCl2+ 2H2O+2NH3↑。(4)A2B是Na2O,由钠离子与氧离子形成的离子化合物,Na2O的形成过程为
CaCl2+ 2H2O+2NH3↑。(4)A2B是Na2O,由钠离子与氧离子形成的离子化合物,Na2O的形成过程为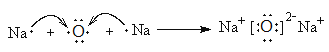 ;(3)M、N均由A、B、C、E四种元素组成,分别是硫酸氢钠和亚硫酸氢钠,两种化合物在水溶液中发生反应的离子方程式为 H++HSO3-=SO2↑+H2O。
;(3)M、N均由A、B、C、E四种元素组成,分别是硫酸氢钠和亚硫酸氢钠,两种化合物在水溶液中发生反应的离子方程式为 H++HSO3-=SO2↑+H2O。

 阅读快车系列答案
阅读快车系列答案