题目内容
【题目】有人认为元素周期表中位于ⅠA族的氢元素,也可以放在ⅦA族.下列物质支持该观点的是( )
A.HF
B.H3O+
C.NaH
D.H2O2
【答案】C
【解析】解:因ⅦA族元素原子在反应中易获得一个电子,显﹣1价,如NaH,氢元素显﹣1价符合题意,A、B、D三项中氢元素均显+1价,不能支持这种观点,故选C.

【题目】常温下,下列各组物质中,Y既能与X反应又能与Z反应的是
X | Y | Z | |
① | NaOH溶液 | Al(OH)3 | 稀硫酸 |
② | KOH溶液液 | Na2CO3 | 稀盐酸 |
③ | CO2 | Na2O2 | H2O |
④ | FeCl3溶液 | Cu | 稀硫酸 |
A. ①③ B. ①④ C. ②④ D. ②③
【题目】[物质结构与性质]氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解。
(1)溴的价电子排布式为 ;PCl3的空间构型为 。
(2)已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列 式发生:
A.CsICl2=CsCl+ICl B.CsICl2=CsI+Cl2
(3)根据下表第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是__________
氟 | 氯 | 溴 | 碘 | |
第一电离能(kJmol﹣1) | 1681 | 1251 | 1140 | 1008 |
(4)下列分子既不存在s﹣pσ键,也不存在p﹣pπ键的是
A. HCl B.HF C. SO2 D. SCl2
(5)已知COCl2为平面形,则COCl2中心碳原子的杂化轨道类型为 ,写出CO的等电子体的微粒 (写出1个)。
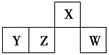
(6)钙在氧气中燃烧时得到一种钙的氧化物晶体,其结构如图所示:由此可判断该钙的氧化物的化学 式为 。已知该氧化物的密度是ρgcm﹣3,则晶胞离得最近的两个钙离子间的距离为 cm(只要求列算式,不必计算出数值,阿伏加德罗常数为NA)。