题目内容
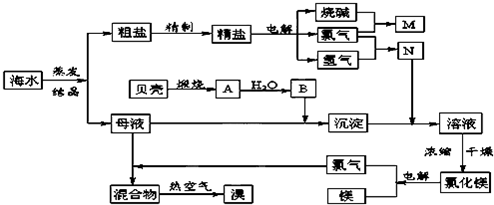
下面涉及的是工业生产硝酸铵的过程。
(1)写出NO2和水反应的化学方程式,并标出电子转移的方向和数目。 。
(2)已知:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H= 一1266.8kJ/mol
N2(g)+O2(g)=2NO(g) △H= +180.5 kJ/mol
写出氨高温催化氧化的热化学方程式: ,
氨催化氧化生成NO反应的化学平衡常数表达式K= 。
(3)已知:N2(g)+3H2(g)
 2NH3(g) △H=-92 kJ/mol。为提高氢气的转化率,宜采取的措施有 。(填字母)
2NH3(g) △H=-92 kJ/mol。为提高氢气的转化率,宜采取的措施有 。(填字母)
A.升高温度 B.使用催化剂
C.及时移出氨 D.循环利用和不断补充氮气
(4)在一定温度和压强下,将H2和N2按3:1(体积比)在密闭容器中混合,当该反应达到平衡时,测得平衡混合气中NH3的气体体积分数为17.6%,此时H2的转化率为 。
(5)许多有机物在特定的装置内进行氧化的同时还可产生电能,这种装置即为燃料电池。
例如,乙烯被氧化生成乙醛的化学反应:2CH2=CH2 + O2 →2CH3CHO可设计成燃料电池:
正极为:O2+4H++4e-=2H2O 负极为:
电池工作时,负极附近溶液的pH (填“升高”、“降低”或“不变”)。
(1)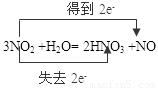 (电子转移省略 )(写出方程式1分,电子转移1分) (2分
)
(电子转移省略 )(写出方程式1分,电子转移1分) (2分
)
(2)4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H=-905.8kJ/mol
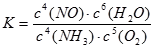
(3)CD
(4)30%(或29.9%)
(5)CH2=CH2+H2O–2e— = CH3CHO+2H+ 降低
【解析】
试题分析:(1)3 mol NO2与水发生反应,有1 mol 被还原为NO,2 mol 被氧化为硝酸,转移电子2 mol,NO2既是氧化剂又是还原剂;(2)根据盖斯定律,消去中间产物氮气可得,K等于生成物浓度的系数次方的乘积除以反应物浓度的系数次方的乘积;(3)提高氢气转化率,就是改变条件让平衡向右移动,结合勒夏特列原理,CD符合; (4)列出三段式,根据氨气的体积分数可得;(5)用总反应减去正极反应可得,负极产生H+,pH降低 。
考点:考查化学反应原理。