题目内容
重铬酸钾是工业生产和实验室的重要氧化剂.工业上常用铬铁矿(主要成份为FeO?Cr2O3)为原料生产K2Cr2O7,其主要工艺如下(涉及的主要反应是:6FeO?Cr2O3+24NaOH+7KClO3
12Na2CrO4+3Fe2O3+7KCl+12H2O):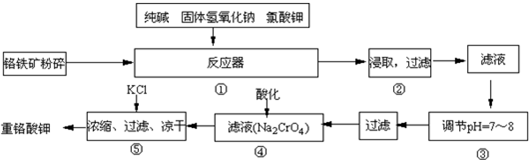
试回答下列问题:
(1)在反应器①中,有Na2CrO4生成,同时Fe2O3转变为NaFeO2,杂质SiO2、Al2O3与纯碱反应转变为可溶性盐,写出氧化铝与碳酸钠反应的化学方程式:
(2)NaFeO2能强烈水解,在操作②生成沉淀而除去,写出该反应的化学方程式:
(3)操作③的目的是什么,用简要的文字说明:
(4)操作④中酸化时,CrO42-转化为Cr2O72-,写出平衡转化的离子方程式:
(5)操作⑤中利用下面的复分解反应,可得重铬酸钾:Na2Cr2O7+2KCl→K2Cr2O7+2NaCl. 试从你所学过的知识分析该反应可以发生的原因:
| ||

试回答下列问题:
(1)在反应器①中,有Na2CrO4生成,同时Fe2O3转变为NaFeO2,杂质SiO2、Al2O3与纯碱反应转变为可溶性盐,写出氧化铝与碳酸钠反应的化学方程式:
Al2O3+Na2CO3
2NaAlO2+CO2↑
| ||
Al2O3+Na2CO3
2NaAlO2+CO2↑
.
| ||
(2)NaFeO2能强烈水解,在操作②生成沉淀而除去,写出该反应的化学方程式:
NaFeO2+2H2O═Fe(OH)3↓+NaOH
NaFeO2+2H2O═Fe(OH)3↓+NaOH
.(3)操作③的目的是什么,用简要的文字说明:
降低pH值有利于的SiO32-,AlO2-水解平衡向正反应方向移动,当pH调到7~8时,使它们水解并沉淀完全
降低pH值有利于的SiO32-,AlO2-水解平衡向正反应方向移动,当pH调到7~8时,使它们水解并沉淀完全
.(4)操作④中酸化时,CrO42-转化为Cr2O72-,写出平衡转化的离子方程式:
2CrO42-+2H+?Cr2O72-+H2O
2CrO42-+2H+?Cr2O72-+H2O
.(5)操作⑤中利用下面的复分解反应,可得重铬酸钾:Na2Cr2O7+2KCl→K2Cr2O7+2NaCl. 试从你所学过的知识分析该反应可以发生的原因:
常温下重铬酸钾的溶解度较小
常温下重铬酸钾的溶解度较小
、温度对氯化钠的溶解度影响很小,但对重铬酸钾的溶解度影响较大,所以将溶液浓缩后,冷却,即有大量重铬酸钾结晶析出,氯化钠仍留在溶液中
温度对氯化钠的溶解度影响很小,但对重铬酸钾的溶解度影响较大,所以将溶液浓缩后,冷却,即有大量重铬酸钾结晶析出,氯化钠仍留在溶液中
.分析:(1)Al2O3与纯碱反应转变为可溶性盐偏铝酸钠和二氧化碳;
(2)NaFeO2能强烈水解,生成氢氧化铁和氢氧化钠;
(3)硅酸钠和偏铝酸钠易发生水解,根据水解平衡移动原理来回答;
(4)在酸性环境下,CrO42-转化为Cr2O72-,据此写出反应的化学方程式;
(5)根据常温下重铬酸钾和重铬酸钠溶解度及温度对氯化钠的影响方面进行分析.
(2)NaFeO2能强烈水解,生成氢氧化铁和氢氧化钠;
(3)硅酸钠和偏铝酸钠易发生水解,根据水解平衡移动原理来回答;
(4)在酸性环境下,CrO42-转化为Cr2O72-,据此写出反应的化学方程式;
(5)根据常温下重铬酸钾和重铬酸钠溶解度及温度对氯化钠的影响方面进行分析.
解答:解:(1)Al2O3与纯碱反应转变为可溶性盐,生成NaAlO2,反应的化学方程式为Al2O3+Na2CO3
2NaAlO2+CO2↑,
故答案为:Al2O3+Na2CO3
2NaAlO2+CO2↑;
(2)NaFeO2能强烈水解,为强碱弱酸液,水解呈碱性,生成氢氧化铁沉淀,反应的离子方程式为FeO2-+2H2O=Fe(OH)3↓+OH-,
故答案为:FeO2-+2H2O=Fe(OH)3↓+OH-;
(3)由于硅酸钠和偏铝酸钠在溶液中发生水解,SiO32-+H2O?HSiO3-+OH-、HSiO3-+H2O?H2SiO3+OH-、AlO2-+2H2O?Al(OH)3+OH-,降低pH有利于水解平衡向正反应方向移动,当pH调到7~8时能使它们完全水解生成沉淀,
故答案为:降低pH值有利于的SiO32-,AlO2-水解平衡向正反应方向移动,当pH调到7~8时,使它们水解并沉淀完全;
(4)在酸性环境下,CrO42-转化为Cr2O72-,即2CrO42-+2H+?Cr2O72-+H2O,
故答案为:2CrO42-+2H+?Cr2O72-+H2O;
(5)由于常温下重铬酸钾的溶解度较小;温度对氯化钠的溶解度影响很小,但对重铬酸钾的溶解度影响较大,所以将溶液浓缩后,冷却,即有大量重铬酸钾结晶析出,氯化钠仍留在溶液中,所以可利用反应Na2Cr2O7+2KCl→K2Cr2O7+2NaCl制得重铬酸钾,
故答案为:常温下重铬酸钾的溶解度较小;温度对氯化钠的溶解度影响很小,但对重铬酸钾的溶解度影响较大,所以将溶液浓缩后,冷却,即有大量重铬酸钾结晶析出,氯化钠仍留在溶液中.
| ||
故答案为:Al2O3+Na2CO3
| ||
(2)NaFeO2能强烈水解,为强碱弱酸液,水解呈碱性,生成氢氧化铁沉淀,反应的离子方程式为FeO2-+2H2O=Fe(OH)3↓+OH-,
故答案为:FeO2-+2H2O=Fe(OH)3↓+OH-;
(3)由于硅酸钠和偏铝酸钠在溶液中发生水解,SiO32-+H2O?HSiO3-+OH-、HSiO3-+H2O?H2SiO3+OH-、AlO2-+2H2O?Al(OH)3+OH-,降低pH有利于水解平衡向正反应方向移动,当pH调到7~8时能使它们完全水解生成沉淀,
故答案为:降低pH值有利于的SiO32-,AlO2-水解平衡向正反应方向移动,当pH调到7~8时,使它们水解并沉淀完全;
(4)在酸性环境下,CrO42-转化为Cr2O72-,即2CrO42-+2H+?Cr2O72-+H2O,
故答案为:2CrO42-+2H+?Cr2O72-+H2O;
(5)由于常温下重铬酸钾的溶解度较小;温度对氯化钠的溶解度影响很小,但对重铬酸钾的溶解度影响较大,所以将溶液浓缩后,冷却,即有大量重铬酸钾结晶析出,氯化钠仍留在溶液中,所以可利用反应Na2Cr2O7+2KCl→K2Cr2O7+2NaCl制得重铬酸钾,
故答案为:常温下重铬酸钾的溶解度较小;温度对氯化钠的溶解度影响很小,但对重铬酸钾的溶解度影响较大,所以将溶液浓缩后,冷却,即有大量重铬酸钾结晶析出,氯化钠仍留在溶液中.
点评:考查学生对工艺流程理解、实验操作的理解、阅读题目获取信息能力、盐类水解及有关计算、电离等,难度中等,理解工艺流程是关键,需要学生具有阅读题目获取信息能力和灵活运用基础知识分析问题、解决问题能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
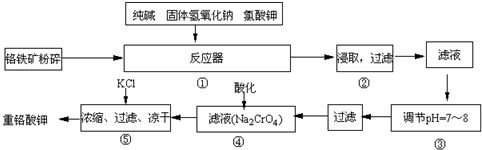
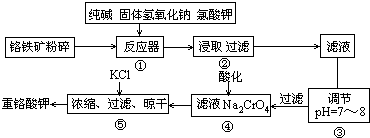
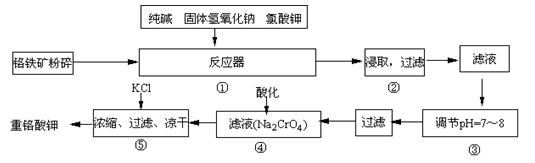
 12Na2CrO4+3Fe2O3
+7KCl+12H2O,
12Na2CrO4+3Fe2O3
+7KCl+12H2O,