题目内容
.海水中含有丰富的化学元素,下面是某化工厂从海水中提取NaCl、Mg(以MgCl2形式存在)和Br2(以NaBr的形式存在)及综合利用的生产流程简图:
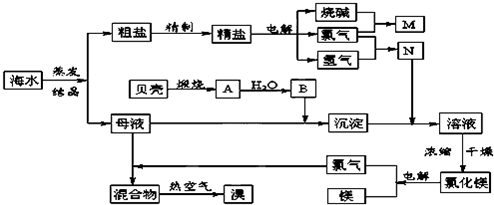
请回答:
(1)在粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂为:
A.盐酸 B.氯化钡溶液 C.氢氧化钠溶液 D.碳酸钠溶液.
则加入试剂的顺序是(填编号)
(2)Mg(OH)2中加入盐酸后,要获得MgCl2?6H2O晶体,需要进行的实验操作依次
A.蒸馏 B.灼烧 C.过滤 D.蒸发 E.冷却结晶
(3)目前工业上主要采用离子交换膜法电解饱和食盐水,下列关于离子交换膜电解槽的叙述错误的是
A.精制饱和食盐水进入阳极室 B.纯水(加少量NaOH)进入阴极室
C.阴极产物为氢氧化钠和氢气 D.电解槽的阳极用金属铁网制成
(4)写出电解饱和NaCl溶液的电极反应方程式:
(5)此工业煅烧贝壳得到氧化钙.石灰石和贝壳的主要成份相同,事实上,石灰石在许多化学工业生产都发挥了极大的作用,请写出一条化工生产中碳酸钙参与的化学反应方程式(此工业涉及的方程式除外)
(6)利用MgCl2?6H2O可制得无水氯化镁,应采取的措施是
(7)用热空气吹出的溴蒸气可以用亚硫酸钠溶液吸收,写出反应的化学方程式:

请回答:
(1)在粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂为:
A.盐酸 B.氯化钡溶液 C.氢氧化钠溶液 D.碳酸钠溶液.
则加入试剂的顺序是(填编号)
C B D A或B C D A
C B D A或B C D A
.(2)Mg(OH)2中加入盐酸后,要获得MgCl2?6H2O晶体,需要进行的实验操作依次
DEC
DEC
.A.蒸馏 B.灼烧 C.过滤 D.蒸发 E.冷却结晶
(3)目前工业上主要采用离子交换膜法电解饱和食盐水,下列关于离子交换膜电解槽的叙述错误的是
D
D
.A.精制饱和食盐水进入阳极室 B.纯水(加少量NaOH)进入阴极室
C.阴极产物为氢氧化钠和氢气 D.电解槽的阳极用金属铁网制成
(4)写出电解饱和NaCl溶液的电极反应方程式:
2Cl--2e-═Cl2↑:2H++2e-═H2↑;
2Cl--2e-═Cl2↑:2H++2e-═H2↑;
.(5)此工业煅烧贝壳得到氧化钙.石灰石和贝壳的主要成份相同,事实上,石灰石在许多化学工业生产都发挥了极大的作用,请写出一条化工生产中碳酸钙参与的化学反应方程式(此工业涉及的方程式除外)
CaCO3+SiO2
CaSiO3+CO2
| ||
CaCO3+SiO2
CaSiO3+CO2
.
| ||
(6)利用MgCl2?6H2O可制得无水氯化镁,应采取的措施是
要在HCl气流中脱水,
要在HCl气流中脱水,
.(7)用热空气吹出的溴蒸气可以用亚硫酸钠溶液吸收,写出反应的化学方程式:
2Na2SO3+Br2+H2O=2Na2SO4+2HBr
2Na2SO3+Br2+H2O=2Na2SO4+2HBr
.分析:(1)根据镁离子用氢氧根离子沉淀,硫酸根离子用钡离子沉淀,钙离子用碳酸根离子沉淀,过滤要放在所有的沉淀操作之后,加碳酸钠要放在加氯化钡之后,可以将过量的钡离子沉淀最后再用盐酸处理溶液中的碳酸根离子和氢氧根离子进行分析;
(2)Mg(OH)2中加入盐酸后,要获得MgCl2?6H2O晶体,需要进行的实验操作为:蒸发浓缩,冷却结晶.如果要使该晶体变为无水氯化镁,一定要在HCl气氛中脱水,否则会水解;
(3)离子交换膜法电解饱和食盐水,电解饱和食盐时阳极阴离子Cl-、OH-放电,Cl-的放电能力强于OH-,阳极发生的方程式为:2Cl--2e-═Cl2↑,阴极:2H++2e-═H2↑;H2、NaOH在阴极,NaOH溶液的出口为阴极,Cl2在阳极生成,精制饱和食盐水从阳极进入;
(4)电解饱和食盐时阳极阴离子Cl-、OH-放电,Cl-的放电能力强于OH-,电解饱和NaCl溶液的电极反应方程式,
阳极发生的方程式为:2Cl--2e-═Cl2↑,阴极:2H++2e-═H2↑;
(5)碳酸钙可以在制玻璃工业中、工业炼铁等;
(6)利用MgCl2?6H2O可制得无水氯化镁,要在HCl气氛中脱水;
(7)用热空气吹出的溴蒸气可以用亚硫酸钠溶液吸收,发生的反应是亚硫酸钠被溴单质氧化为硫酸钠;
(2)Mg(OH)2中加入盐酸后,要获得MgCl2?6H2O晶体,需要进行的实验操作为:蒸发浓缩,冷却结晶.如果要使该晶体变为无水氯化镁,一定要在HCl气氛中脱水,否则会水解;
(3)离子交换膜法电解饱和食盐水,电解饱和食盐时阳极阴离子Cl-、OH-放电,Cl-的放电能力强于OH-,阳极发生的方程式为:2Cl--2e-═Cl2↑,阴极:2H++2e-═H2↑;H2、NaOH在阴极,NaOH溶液的出口为阴极,Cl2在阳极生成,精制饱和食盐水从阳极进入;
(4)电解饱和食盐时阳极阴离子Cl-、OH-放电,Cl-的放电能力强于OH-,电解饱和NaCl溶液的电极反应方程式,
阳极发生的方程式为:2Cl--2e-═Cl2↑,阴极:2H++2e-═H2↑;
(5)碳酸钙可以在制玻璃工业中、工业炼铁等;
(6)利用MgCl2?6H2O可制得无水氯化镁,要在HCl气氛中脱水;
(7)用热空气吹出的溴蒸气可以用亚硫酸钠溶液吸收,发生的反应是亚硫酸钠被溴单质氧化为硫酸钠;
解答:(1)镁离子用氢氧根离子沉淀,加入过量的石灰乳可以将镁离子沉淀,硫酸根离子用钡离子沉淀,加入过量的氯化钡可以将硫酸根离子沉淀,至于先除镁离子,还是先除硫酸根离子都行,钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,离子都沉淀了,在进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,所以添加试剂的顺序为:CBDA;或BCDA;
(2)Mg(OH)2中加入盐酸后,要获得MgCl2?6H2O晶体,需要进行的实验操作为:蒸发浓缩,冷却结晶.如果要使该晶体变为无水氯化镁,一定要在HCl气氛中脱水,否则会水解;
故答案为:DEC;
(3)目前工业上主要采用离子交换膜法电解饱和食盐水,电解饱和食盐时阳极阴离子Cl-、OH-放电,Cl-的放电能力强于OH-,
阳极:2Cl--2e-═Cl2↑,
阴极:2H++2e-═H2↑;
总反应为:2NaCl+2H2O
Cl2↑+H2↑+2NaOH,
阴极:氢离子放电,产生氢气.致使氢氧根离子浓度增大,钠离子和氢氧根离子的增大都发生在阴极室,所以阴极出口导出的液体是氢氧化钠溶液;
阳极:氯离子放电,产生氯气,致使钠离子浓度升高,通过阳离子交换膜到达阴极室.所以阳极入口应加入精制饱和食盐水;
故答案为:D;
(4)电解饱和食盐时阳极阴离子Cl-、OH-放电,Cl-的放电能力强于OH-,阳极:2Cl--2e-═Cl2↑,阴极:2H++2e-═H2↑;
故答案为:2Cl--2e-═Cl2↑:2H++2e-═H2↑;
(5)工业炼铁除硫磷:CaCO3+SO2═CaSO3+CO2;工业制玻璃反应原理;CaCO3+SiO2
CaSiO3+CO2
故答案为:CaCO3+SiO2
CaSiO3+CO2
(6)利用MgCl2?6H2O可制得无水氯化镁,应采取的措施是,在HCl气流中加热脱水,故答案为:在HCl气流中加热脱水;
(7)用热空气吹出的溴蒸气可以用亚硫酸钠溶液吸收,发生的反应是亚硫酸钠被溴单质氧化为硫酸钠;反应的化学方程式为:2Na2SO3+Br2+H2O=2Na2SO4+2HBr;
故答案为:2Na2SO3+Br2+H2O=2Na2SO4+2HBr;
(2)Mg(OH)2中加入盐酸后,要获得MgCl2?6H2O晶体,需要进行的实验操作为:蒸发浓缩,冷却结晶.如果要使该晶体变为无水氯化镁,一定要在HCl气氛中脱水,否则会水解;
故答案为:DEC;
(3)目前工业上主要采用离子交换膜法电解饱和食盐水,电解饱和食盐时阳极阴离子Cl-、OH-放电,Cl-的放电能力强于OH-,
阳极:2Cl--2e-═Cl2↑,
阴极:2H++2e-═H2↑;
总反应为:2NaCl+2H2O
| ||
阴极:氢离子放电,产生氢气.致使氢氧根离子浓度增大,钠离子和氢氧根离子的增大都发生在阴极室,所以阴极出口导出的液体是氢氧化钠溶液;
阳极:氯离子放电,产生氯气,致使钠离子浓度升高,通过阳离子交换膜到达阴极室.所以阳极入口应加入精制饱和食盐水;
故答案为:D;
(4)电解饱和食盐时阳极阴离子Cl-、OH-放电,Cl-的放电能力强于OH-,阳极:2Cl--2e-═Cl2↑,阴极:2H++2e-═H2↑;
故答案为:2Cl--2e-═Cl2↑:2H++2e-═H2↑;
(5)工业炼铁除硫磷:CaCO3+SO2═CaSO3+CO2;工业制玻璃反应原理;CaCO3+SiO2
| ||
故答案为:CaCO3+SiO2
| ||
(6)利用MgCl2?6H2O可制得无水氯化镁,应采取的措施是,在HCl气流中加热脱水,故答案为:在HCl气流中加热脱水;
(7)用热空气吹出的溴蒸气可以用亚硫酸钠溶液吸收,发生的反应是亚硫酸钠被溴单质氧化为硫酸钠;反应的化学方程式为:2Na2SO3+Br2+H2O=2Na2SO4+2HBr;
故答案为:2Na2SO3+Br2+H2O=2Na2SO4+2HBr;
点评:本题考查了海水资源的综合利用,工业生产流程的分析判断,电解原理的应用,电极名称,电极产物,电极反应的应用,粗盐的提纯步骤,晶体的提纯方法,题目内容综合性较强,难度较大.

练习册系列答案
相关题目