题目内容
16.下列有机物符合最简式为CH2的是( )| A. | C3H8 | B. | C2H6 | C. | CH4 | D. | C4H8 |
分析 最简式又称实验式或经验式,是化学式中的一种,是用元素符号表示化合物分子中各元素的原子个数比的最简关系式,据此计算出各选项中该有机物的最简式即可.
解答 解:A.C3H8分子式为C3H8,最简式为C3H8,故A错误;
B.C2H6分子式为C2H6,最简式为CH3,故B错误;
C.CH4分子式为CH4,最简式为CH4,故C错误;
D.C4H8分子式为C4H8,最简式为CH2,故D正确.
故选D.
点评 本题考查了有机物的最简式,题目难度不大,注意明确最简式的根据及求算方法,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
6. 已知:3CH4(g)+2N2(g)?3C(s)+4NH3(g)△H>0,700℃时,CH4与N2在不同物质的量之比[n(CH4)/n(N2)]时CH4的平衡转化率如图所示,下列说法不正确的是( )
已知:3CH4(g)+2N2(g)?3C(s)+4NH3(g)△H>0,700℃时,CH4与N2在不同物质的量之比[n(CH4)/n(N2)]时CH4的平衡转化率如图所示,下列说法不正确的是( )
 已知:3CH4(g)+2N2(g)?3C(s)+4NH3(g)△H>0,700℃时,CH4与N2在不同物质的量之比[n(CH4)/n(N2)]时CH4的平衡转化率如图所示,下列说法不正确的是( )
已知:3CH4(g)+2N2(g)?3C(s)+4NH3(g)△H>0,700℃时,CH4与N2在不同物质的量之比[n(CH4)/n(N2)]时CH4的平衡转化率如图所示,下列说法不正确的是( )| A. | n(CH4)/n(N2)越小,CH4的转化率越高 | |
| B. | n(CH4)/n(N2)不变时,若升温,NH3的体积分数会增大 | |
| C. | b点对应的平衡常数与a点一样 | |
| D. | a点对应的NH3的体积分数约为26% |
7.下列各化合物的命名正确的是( )
| A. | CH2=CH-CH=CH2 1,3-二丁烯 | B. |  3-丁醇 3-丁醇 | ||
| C. | 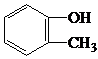 甲基苯酚 甲基苯酚 | D. | 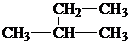 2-甲基丁烷 2-甲基丁烷 |
1.以下化学用语正确的是( )
| A. | 熟石膏的化学式:2CaSO4•H2O | B. | 明矾的化学式KAlSO4•12H2O | ||
| C. | CaCl2的电子式: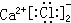 | D. | 氯化钠的电子式Na:$\underset{\stackrel{..}{Cl}}{..}$: |
8.下列不正确的是( )
| A. | 酸性:HClO4>HBrO4>HIO4 | B. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | ||
| C. | 稳定性:PH3>H2S>HCl | D. | 非金属性:F>O>S |
5.下列各组粒子能在指定溶液中大量共存的是( )
| A. | 银氨溶液中:Na+,H+,NO3- | B. | 碘化钾溶液中:H+,H2O,SO32- | ||
| C. | 偏铝酸钠溶液中:K+,Cl-,SO42- | D. | 氢氧化钙溶液中:Na+,ClO-,HCO3- |
6.元素周期表是学习化学的重要工具,它隐含着许多信息和规律.下面是八种短周期元素的相关信息(已知铍的原子半径为0.089nm)
F原子中无中子,G最高正价数与负价数相等,且最外层电子数是次外层的二倍,H元素单质焰色反应呈黄色.
(1)B元素在元素周期表中的位置第三周期第ⅢA族B形成的简单离子的结构示意图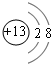 .
.
(2)上述元素的最高价氧化物对应的水化物中酸性最强的是H2SO4.
(3)用电子式表示C、H形成化合物的过程: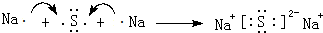 .
.
(4)H、E形成原子个数比为1:1的化合物中所含化学键类型为离子键和非极性键.
(5)G的最高价与E形成的化合物的电子式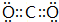 ,该分子的结构式为O=C=O.
,该分子的结构式为O=C=O.
(6)A、B、C、E原子半径由大到小的顺序为Mg>Al>S>O.
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | -1 | -2 |
(1)B元素在元素周期表中的位置第三周期第ⅢA族B形成的简单离子的结构示意图
 .
.(2)上述元素的最高价氧化物对应的水化物中酸性最强的是H2SO4.
(3)用电子式表示C、H形成化合物的过程:
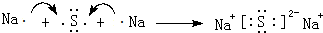 .
.(4)H、E形成原子个数比为1:1的化合物中所含化学键类型为离子键和非极性键.
(5)G的最高价与E形成的化合物的电子式
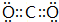 ,该分子的结构式为O=C=O.
,该分子的结构式为O=C=O.(6)A、B、C、E原子半径由大到小的顺序为Mg>Al>S>O.
 把在空气中久置的铝片5.0g投入盛有500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间(单位:秒)的关系可用如图曲线来表示,回答下列问题:
把在空气中久置的铝片5.0g投入盛有500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间(单位:秒)的关系可用如图曲线来表示,回答下列问题: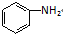 )、水杨酸(
)、水杨酸(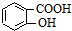 )、硝基苯与苯酚四种有机物的乙醚溶液,按如下流程利用物质的酸碱性依次分离,假设每一步分离都是完全的.(已知苯胺是一种难溶于水,具有弱碱性的有机物.)
)、硝基苯与苯酚四种有机物的乙醚溶液,按如下流程利用物质的酸碱性依次分离,假设每一步分离都是完全的.(已知苯胺是一种难溶于水,具有弱碱性的有机物.)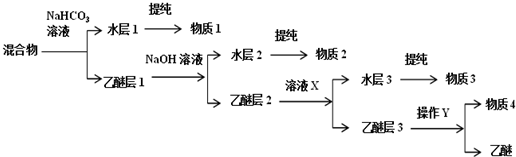
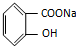 ,物质3的分子式为C6H7N.
,物质3的分子式为C6H7N. .
.