题目内容
【题目】常温下,用0.100mol/L 的AgNO3溶液滴定50.0mL,0.0500mol/L KCl溶液,以K2CrO4为指示剂,测得溶液中pCl=-lgc(Cl-) 、pAg=-lgc(Ag+)随加入AgNO3的体积变化如图所示,已知溶液中离子浓度小于等于1.0×10-5mol/L则沉淀完全,Ksp(Ag2CrO4)=2.0×10-12,Ksp(Ag2SO4)=1.4×10-5,下列说法错误的是( )

A. AgCl的沉淀溶解平衡常数Ksp数量级为10-10
B. 为防止指示剂失效,溶液应维持中性或弱碱性
C. 滴定中指示剂的有效浓度应维持在2.0×10-2 mol/L
D. 滴定完后加入1mL 0.01mol/L H2SO4会产生新的沉淀
【答案】D
【解析】A.根据图像,硝酸银溶液的体积为25mL时,pAg=pCl =5,则AgCl的沉淀溶解平衡常数Ksp=1.0×10-5×1.0×10-5= 10-10,故A正确;B. K2CrO4中存在2CrO4 2-+ 2H+ =Cr2O7 2-+ H2O平衡,为防止指示剂失效,溶液应维持中性或弱碱性,故B正确;C. 溶液中离子浓度小于等于1.0×10-5mol/L则沉淀完全,因此沉淀完全时,溶液中的c(Cl-)=c(Ag+)=1.0×10-5 mol/L,滴定中指示剂的有效浓度应维持在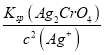 =
=![]() =2.0×10-2 mol/L,故C正确;D. 滴定完溶液中的c(Ag+)=1.0×10-5 mol/L,后加入1mL0.01mol/L H2SO4,c(SO42-)=
=2.0×10-2 mol/L,故C正确;D. 滴定完溶液中的c(Ag+)=1.0×10-5 mol/L,后加入1mL0.01mol/L H2SO4,c(SO42-)=![]() ≈0.004 mol/L,此时Qc= c2(Ag+)×c(SO42-)=4×10-13<1.4×10-5,不会产生新的沉淀,故D错误;故选D。
≈0.004 mol/L,此时Qc= c2(Ag+)×c(SO42-)=4×10-13<1.4×10-5,不会产生新的沉淀,故D错误;故选D。

 春雨教育同步作文系列答案
春雨教育同步作文系列答案【题目】一种从含Br-废水中提取Br2的过程,包括过滤、氧化、正十二烷萃取及蒸馏等步骤。己知:
Br2 | CCl4 | 正十二烷 | |
密度/g·cm-3 | 3.119 | 1.595 | 0.753 |
沸点/℃ | 58.76 | 76.8 | 215~217 |
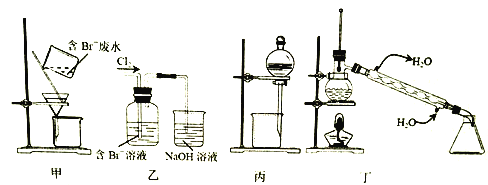
下列说法正确的是
A. 用甲装置过滤时,需不断搅拌
B. 丙装置中用正十二烷而不用CCl4,是因为其密度小
C. 用乙装置将Br-氧化为Br2
D. 可用装置丁进行蒸馏,先收集正十二烷再收集Br2