题目内容
【题目】(1)第ⅢB族有_____种元素,第117号元素属于_________元素(填“金属”或“非金属”);
(2)第5周期第ⅤA族元素的元素名称为_________,原子序数为_______;
(3)第4周期元素硒的某一核素含有46个中子,该元素的原子符号为_______;
(4)![]() 和
和![]() 是元素X的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为W g,则
是元素X的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为W g,则![]() 的相对原子质量为___________,元素X的近似相对原子质量为______________________。
的相对原子质量为___________,元素X的近似相对原子质量为______________________。
【答案】 32 金属 锑 51 ![]()
![]() A×m%+B×n%
A×m%+B×n%
【解析】分析:(1)根据元素周期表的结构分析;
(2)根据元素周期表的结构分析;
(3)根据硒的质子数计算质量数,进而书写该核素的原子符号;
(4)原子的相对原子质量是一个原子的真实质量与一个![]() 原子质量的
原子质量的![]() 的比值;元素的相对原子质量是该元素各种核素原子的相对原子质量与其在自然界中所占原子个数百分比的乘积之和。
的比值;元素的相对原子质量是该元素各种核素原子的相对原子质量与其在自然界中所占原子个数百分比的乘积之和。
详解:(1)第ⅢB族由于含有镧系和錒系,因此有32种元素,第117号元素位于第七周期第ⅦA,因此属于金属元素;
(2)第5周期第ⅤA族元素的元素名称为锑,氮元素的原子序数是7,则锑的原子序数为7+8+18+18=51;
(3)第4周期元素硒的质子数是8+8+18=34,若某一核素含有46个中子,则该核素的质量数是34+46=80,因此该元素的原子符号为![]() ;
;
(4)已知12C原子的质量为W g,则![]() 的相对原子质量为
的相对原子质量为![]() 。核素的近似相对原子质量可以看作是质量数,则元素X的近似相对原子质量为A×m%+B×n%。
。核素的近似相对原子质量可以看作是质量数,则元素X的近似相对原子质量为A×m%+B×n%。

【题目】锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛.回答下列问题:
(1)基态Ge原子的核外电子排布式为[Ar] , 有个未成对电子.
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键.从原子结构角度分析,原因是 .
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因 .
GeCl4 | GeBr4 | GeI4 | |
熔点/℃ | ﹣49.5 | 26 | 146 |
沸点/℃ | 83.1 | 186 | 约400 |
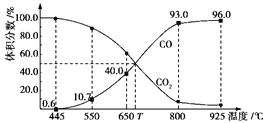
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂.Zn、Ge、O电负性由大至小的顺序是 .
(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为微粒之间存在的作用力是 .
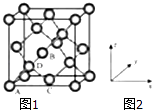
(6)晶胞有两个基本要素:①原子坐标参数,表示晶胞内部各原子的相对位置,如图(1、2)为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为( ![]() ,0,
,0, ![]() );C为(
);C为( ![]() ,
, ![]() ,0).则D原子的坐标参数为 .
,0).则D原子的坐标参数为 .
②晶胞参数,描述晶胞的大小和形状,已知Ge单晶的晶胞参数a=565.76pm,其密度为gcm﹣3(列出计算式即可).