题目内容
【题目】铜及其化合物在工农业生产有着重要的用途,氯化铜、氯化业铜经常用作催化剂。其中CuCl广泛应用于化工和印染等行业。
【查阅资料】(i)氯化铜:从水溶液中结晶时,在15℃以下得到四水物,在15-25.7℃得到三水物,在26~42℃得到二水物,在42℃以上得到一水物,在100得到无水物。
(ii)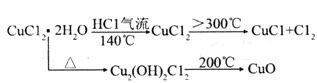
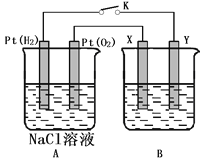
(1)实验室用如图所示的实验仪器及药品制备纯净、干燥的氧气并与铜反应(铁架台,铁夹略)制备氯化铜。

①按气流方向连接各仪器接口顺序是:
a→_____、_____→_____、_____→_____、_____→_____。
②本套装置有两个仪器需要加热,加热的顺序为先_____后_______
(2)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,写出该反应的化学方程式:_____________________。
(3)现欲从(2)所得溶液获得纯净的CuCl22H2O,进行如下操作:
①首先向溶液中加入H2O2溶液然后再加试剂X用于调节pH,过滤,除去杂质,X可选用下列试剂中的(填序号)
a.NaOH b.NH3H2O C.CuO d.CuSO4
②要获得纯净CuCl22H2O晶体的系列操作步骤为:向①所得滤液中加少量盐酸,蒸发浓缩、_____、_____、洗涤、干燥。
(4)用CuCl22H2O为原料制备CuCl时,发现其中含有少量的CuCl2或CuO杂质,若杂质是CuCl2,则产生的原因是______________。
(5)设计简单的实验验证0.1mol/L的CuCl2溶液中的Cu2+对H2O2的分解具有催化作用:_____。
【答案】 d e h i f g b AD 2FeCl3+Cu=2FeCl2+CuCl2 c 冷却到26-42℃结晶(只答冷却结晶不得分) 过滤 加热温度低(加热时间不够) 取两支试管加入等体积等浓度的过氧化氢溶液一支加入几滴0.1mol/L的CuCl2溶液另一支加入几滴0.2mol/L的NaCl溶液滴加氧化铜溶液的试管产生的气泡速率快(其它合理答案也可)
【解析】试题分析:本题考查Cl2的实验室制备、装置的连接、物质的除杂、基本实验操作、实验方案的设计。
(1)①用装置A制备Cl2,制得的Cl2中混有HCl、H2O(g),所以将气体先通过盛饱和食盐水的装置C除去HCl,再通过盛浓H2SO4的装置E干燥Cl2,用纯净、干燥的Cl2与Cu反应制备CuCl2;由于Cl2会污染大气,最后用盛放NaOH溶液的装置B吸收尾气;同时注意洗气时导气管应长进短出;按气流方向连接各仪器接口顺序是:a→d、e→h、i→f、g→b。
②实验室用MnO2和浓盐酸加热制Cl2,Cu与Cl2加热反应制备CuCl2,则装置A和装置D需要加热;为了防止Cu与空气中的O2反应生成CuO,所以实验时必须先加热装置A产生Cl2,用生成的Cl2赶尽装置中的空气后再加热装置D。
(2)Cu与FeCl3溶液反应生成CuCl2和FeCl2,反应的化学方程式为Cu+2FeCl3=CuCl2+2FeCl2。
(3)①向(2)所得溶液中加入H2O2溶液将Fe2+氧化成Fe3+,加入试剂X调节pH除去Fe3+。a项,加入NaOH可调节pH除去Fe3+,但引进新杂质Na+;b项,加入NH3·H2O可调节pH除去Fe3+,但引进新杂质NH4+;c项,加入CuO可调节pH除去Fe3+,且不引入新杂质;d项,加入CuSO4不能除去Fe3+;答案选c。
②根据题给资料(i)要获得CuCl2·2H2O需控制温度在26~42℃,所以要获得纯净CuCl2·2H2O晶体的系列操作步骤为:向①所得滤液中加少量盐酸,蒸发浓缩、冷却到26~42℃结晶、过滤、洗涤、干燥。
(4)根据资料(ii),CuCl2·2H2O在HCl气流中加热到140℃失去结晶水生成CuCl2,继续加热到温度![]() 300℃时生成CuCl和Cl2,若发现CuCl中含有杂质CuCl2,产生的原因是:加热温度低(或加热时间不够)。
300℃时生成CuCl和Cl2,若发现CuCl中含有杂质CuCl2,产生的原因是:加热温度低(或加热时间不够)。
(5)要证明0.1mol/LCuCl2溶液中的Cu2+对H2O2的分解具有催化作用采用控制变量法,控制H2O2等浓度、等体积,两溶液中Cl-浓度相同;设计的简单实验为:取两支试管,加入等体积、等浓度的H2O2溶液,一支加入几滴0.1mol/L的CuCl2溶液,另一支加入几滴0.2mol/L的NaCl溶液,滴加CuCl2溶液的试管产生气泡速率快,说明Cu2+对H2O2的分解具有催化作用。

 阅读快车系列答案
阅读快车系列答案