题目内容
铋(Bi)在医药方面有重要应用。下列关于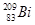 i和
i和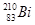 的说法正确的是
的说法正确的是
A.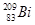 i和 i和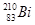 都含有83个中子 都含有83个中子 |
B.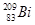 和 和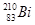 互为同位素 互为同位素 |
C.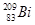 i和 i和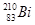 的核外电子数不同 的核外电子数不同 |
D.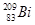 i和 i和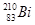 都含有83个质子,是同一种核素 都含有83个质子,是同一种核素 |
B
解析试题分析:在表示原子组成时元素符号的左下角表示质子数,左上角表示质量数。A、因为质子数和中子数之和是质量数,所以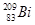 和
和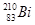 含有的中子数分别是209-83=126、210-83=128,A不正确;B、
含有的中子数分别是209-83=126、210-83=128,A不正确;B、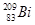 和
和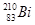 的质子数相同,但中子数不同,二者互为同位素,B正确;C、
的质子数相同,但中子数不同,二者互为同位素,B正确;C、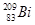 和
和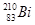 的质子数相同,由于质子数=核外电子数,所以二者的核外电子数也是相同的,C不正确;D、
的质子数相同,由于质子数=核外电子数,所以二者的核外电子数也是相同的,C不正确;D、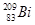 和
和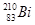 都含有83个质子,但中子数不同,属于不同种核素,D不正确,答案选B。
都含有83个质子,但中子数不同,属于不同种核素,D不正确,答案选B。
考点:考查原子组成以及组成原子的微粒之间数量关系的计算;同位素判断

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法正确的是 ( )
| A.同周期的IA族元素的金属性比IIA族的元素金属性强 |
| B.第三周期元素的阴离子半径从左到右逐渐增大 |
| C.VIA族的气态氢化物一定比VA族的稳定性强 |
| D.原子晶体的熔点一定比离子晶体的高 |
X、Y、Z、W是短周期元素,X元素原子的最外层未达到8电子稳定结构,工业上通过分离液态空气获得其单质;Y元素原子最外电子层上s、p电子数相等;Z元素+2价阳离子的核外电子排布与氖原子相同;W元素原子的M层有1个未成对的p电子。下列有关这些元素性质的说法一定正确的是
| A.X元素的氢化物的水溶液显碱性 |
| B.Z元素的离子半径大于W元素的离子半径 |
| C.Z元素的单质在一定条件下能与X元素的单质反应 |
| D.Y元素最高价氧化物的晶体具有很高的熔点和沸点 |
短周期主族元素X、Y、Z、W、Q的原子序数依次增大,X的气态氢化物极易溶于Y的氢化物中,常温下,Z的单质能溶于W的最高价氧化物的水化物的稀溶液,却不溶于其浓溶液。下列说法不正确的是
| A.离子半径的大小顺序为Z>W>Q |
| B.元素W的气态氢化物与Y的单质可发生置换反应 |
| C.元素X与Y能在一定条件下发生化合反应,说明Y的非金属性比X强 |
| D.元素Z、W、Q的单质在一定条件下均能和强碱溶液反应 |
下列说法中正确的是
| A.电子云通常是用小黑点来表示电子的多少 |
| B.处于最低能量的原子叫基态原子 |
| C.能量高的电子在离核近的区域运动,能量低的电子在离核远的区域运动 |
| D.电子仅在激发态跃迁到基态时才会产生原子光谱 |
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知:
| W | X | |
| | Y | Z |
A.X、Y、Z中最简单氢化物稳定性最弱的是Y
B.Z元素氧化物对应水化物的酸性一定强于Y
C.X元素形成的单核阴离子还原性大于Y
D.Z元素单质在化学反应中只表现氧化性
下列说法正确的是
A.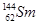 与 与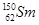 互为同位素 互为同位素 |
| B.氯气能使潮湿的蓝布条变为白色,说明氯气有漂白性 |
| C.将1体积c1mol/L的硫酸用水稀释为5体积,稀溶液的浓度为0.2c1mol/L |
| D.焰色反应一定发生化学变化 |
镭是元素周期表中第7周期第IIA族元素,下列有关叙述不正确的是
| A.镭的金属性比钙弱 | B.单质能与水反应生成H2 |
| C.镭在化合物中呈+2价 | D.碳酸镭难溶于水 |