题目内容
【题目】某二元酸(化学式用H2X表示)在水中的电离方程式是:H2X=H++HX- HX-![]() H++X2-,常温下,向10 mL 0.1000 mol/L的H2X溶液中逐滴加入0.1000 mol/L的NaOH溶液,pH随NaOH溶液体积的变化如图所示。下列叙述中正确的是
H++X2-,常温下,向10 mL 0.1000 mol/L的H2X溶液中逐滴加入0.1000 mol/L的NaOH溶液,pH随NaOH溶液体积的变化如图所示。下列叙述中正确的是

A.a点pH>1
B.b点溶液中:c(Na+)>c(HX-)>c(X2-)>c(H2X)>c(H+)>c(OH-)
C.d点溶液中:c(Na+)=2c(X2-)+2c(HX-)
D.水的电离程度:c>a>e
【答案】D
【解析】
A. 由于该二元酸第一步为完全电离,故a点pH<1,A错误;
B. b点溶液相当于一份NaHX溶液,由于HX-的电离程度大于其水解程度,则b点溶液中c(Na+)>c(HX-) >c(H+)>c(X2-)>c(H2X) >c(OH-),B错误;
C. c点溶液相当于Na2X溶液,可写出溶液中的物料守恒,c(Na+)=2c(X2-)+2c(HX-)+2c(H2X),故C错误;
D. a点相当于在水溶液中加入了10 mL 0.1000 mol/L的H2X溶液,e点相当于加入了20mL 0.1000 mol/L NaOH溶液,故a点的氢离子浓度略大于e点的氢氧根离子浓度,导致对水电离的抑制增加,故水的电离程度c>a>e,D正确;
故答案选D。

【题目】回答下列问题:
1L海水在逐渐浓缩过程中析出盐的种类和质量(单位:g)的关系如下表所示:
海水密度(gmL-1) | CaSO4 | NaCl | MgCl2 | MgSO4 | NaBr |
1.21 | 0.05 | 3.26 | 0.004 | 0.008 | — |
1.22 | 0.015 | 9.65 | 0.01 | 0.012 | — |
1.26 | 0.01 | 2.64 | 0.02 | 0.02 | 0.04 |
1.31 | — | 1.40 | 0.54 | 0.03 | 0.06 |
注:画“—”的数据少于10-4,可以忽略不计。
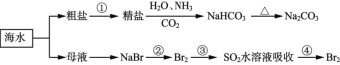
(1)从海水中获得粗盐,一般采用的方法是___。
(2)根据上表,要获得杂质较少的食盐,应控制海水的最佳密度为___gmL-1(填字母)。
A.1.21 B.1.22 C.1.26 D.1.31
(3)粗盐中常含有MgCl2、MgSO4、CaCl2等杂质,要除去这些杂质,按顺序加入的试剂依次为NaOH、BaCl2、___、___等(填化学式)。
(4)工业上电解熔融氯化钠制取金属钠的化学方程式为___。
(5)钠元素的一种常见氧化物可作为呼吸面具的供氧剂,写出该氧化物和CO2反应的化学方程式___。