题目内容
【题目】向 50mL 稀 H2SO4 与稀 HNO3 的混合溶液中逐渐加入铁粉,假设加入铁粉的质量与产生气体的体积(标 准状况下)之间的关系如图所示,且每一段只对应一个反应。下列说法正确的是( )

A. 参加反应铁粉的总质量 m2=5.6 g
B. 所用混合溶液中 c(HNO3)=0.5 molL-1
C. 开始时产生的气体为 H2
D. AB 段产生的反应为置换反应
【答案】A
【解析】已知氧化性:NO3->Fe3+>H+,OA段发生:Fe+NO3-+4H+=Fe3++NO↑+2H2O,AB段发生:Fe+2Fe3+=3Fe2+,B以后发生:Fe+2H+=Fe2++H2↑,则A.最终生成Fe2+,根据氧化还原反应中得失电子数目相等可知3×n(NO)+2×n(H2)=2n(Fe),即3×0.05mol+2×0.56L÷22.4L/mol=2n(Fe),n(Fe)=0.1mol,质量为5.6g,A正确;B.n(NO)=1.12L÷22.4L/mol=0.05mol,则所用混合溶液中c(HNO3)=0.05mol÷0.05L=1mol/L,B错误;C.开始时产生的气体为NO,C错误;D.AB段发生:Fe+2Fe3+=3Fe2+,为化合反应,D错误;答案选A。

【题目】某科研小组设计出利用工业废酸(10%H2SO4)来堆浸某废弃的氧化铜锌矿的方案,实现废物综合利用,方案如图所示. 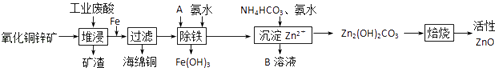
已知:各离子开始沉淀及完全沉淀时的pH如下表所示.
离子 | 开始沉淀时的pH | 完全沉淀时的pH |
Fe2+ | 6.34 | 9.7 |
Fe3+ | 1.48 | 3.2 |
Zn2+ | 6.2 | 8.0 |
请回答下列问题:
(1)氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS不溶,则相同温度下:Ksp(CuS)Ksp(ZnS)(选填“>”“<”或“=”).
(2)物质A可使用下列物质中的 .
A.KMnO4
B.O2
C.H2O2
D.Cl2
(3)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在范围之间.
(4)物质B可直接用作氮肥,则B的化学式是 .
(5)除铁后得到的Fe(OH)3可用KClO溶液在碱性环境将其氧化得到一种高效的多功能水处理剂﹣﹣K2FeO4 , 写出该反应的离子方程式 .