题目内容
3.Z、Y、X、W、V是原子序数依次增大的五种常见元素.X元素是地壳中含量最多的元素,Y、Z组成的气态化合物M的水溶液呈碱性,W的单质在X2中燃烧产物可使品红溶液褪色,V是一种历史悠久、应用广泛的金属元素.请回答:(1)Y元素在周期表中的位置是第二周期第ⅤA族;M的分子空间构型为三角锥形,M是极性分子(“极性”或“非极性”)
(2)写出X、Z两种元素组成的化合物Z2X2的结构式:H-O-O-H.
(3)由以上五种元素两两组合所形成的化合物中,有一种物质能与水反应生成气体且反应属于氧化还原反应,请写出该反应的化学方程式3NO2+H2O=2HNO3+NO.
(4)X、Y、Z三种元素可组成一种强酸U,M与U反应生成一种盐K,写出K中含有的化学键类型离子键、共价键、配位键.
(5)若将V金属投入到盐酸溶液中,生成了浅绿色溶液N.N的酸性溶液与双氧水反应的离子方程式:2Fe2++2H++H2O2=2Fe3++2H2O.
分析 Z、Y、X、W、V是原子序数依次递增的五种常见元素.X元素是地壳中含量最多的元素,则X为O元素;Y、Z组成的气态化合物M的水溶液呈碱性,可推知Y为N元素、Z为H元素,M为NH3;W的单质在X2中燃烧产物可使品红溶液褪色,可推知W为S元素;V是一种历史悠久、应用最广泛的金属元素,(5)中将V金属投入到盐酸溶液中,生成了浅绿色溶液N,则V为Fe元素,N为FeCl2,据此解答.
解答 解:Z、Y、X、W、V是原子序数依次递增的五种常见元素.X元素是地壳中含量最多的元素,则X为O元素;Y、Z组成的气态化合物M的水溶液呈碱性,可推知Y为N元素、Z为H元素,M为NH3;W的单质在X2中燃烧产物可使品红溶液褪色,可推知W为S元素.
(1)Y为N元素,在周期表中的位置是:第二周期第ⅤA族;M为NH3,空间构型为三角锥形,分子中正负电荷重心不重合,属于极性分子,
故答案为:第二周期第ⅤA族; 三角锥;极性;
(2)Z2X2为H2O2,它的结构式为H-O-O-H,故答案为:H-O-O-H;
(3)由以上五种元素两两组合所形成的化合物中,有一种物质能与水反应生成气体且反应属于氧化还原反应,应是二氧化氮与水反应生成硝酸与NO,该反应的化学方程式为:3NO2+H2O=2HNO3+NO,
故答案为:3NO2+H2O=2HNO3+NO;
(4)O、N、H三种元素组成的一种强酸U为HNO3,氨气在适当条件下被HNO3吸收生成NH4NO3,NH4NO3中有离子键和共价键、配位键,
故答案为:离子键、共价键、配位键;
(5)将V金属投入到盐酸溶液中,生成了浅绿色溶液N,则V为Fe元素,N为FeCl2,双氧水具有强氧化性,酸性条件下将亚铁离子氧化为铁离子,同时生成水,FeCl2的酸性溶液与双氧水反应的离子方程式为:2Fe2++2H++H2O2=2Fe3++2H2O,
故答案为:2Fe2++2H++H2O2=2Fe3++2H2O.
点评 本题考查结构性质位置关系应用,题目难度中等,推断元素的种类是关键,注意对基础知识的积累掌握.

| A. | 缩小容器的体积使压强增大 | B. | 体积不变,充入N2 | ||
| C. | 恒容,充入He | D. | 降低反应温度 |
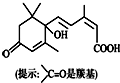
| A. | 其分子式为C15H22O4 | |
| B. | 一定条件下,l mol该有机物最多可与4 mol氢气发生加成反应 | |
| C. | 1 mol该物质与足量NaOH溶液反应,最多消耗2 mol NaOH | |
| D. | 既可以与FeCl3溶液发生显色反应,又可以使酸性KMnO4溶液褪色 |
| A. | 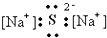 | B. |  | C. |  | D. |  |
| A. | 将SO2通入BaCl2溶液中至饱和,无沉淀产生,再通入过量NH3,产生沉淀 | |
| B. | 高纯硅常用作光导纤维的原料 | |
| C. | 用AlCl3溶液制取Al(OH)3,沉淀剂选用氨水比选用NaOH溶液好 | |
| D. | 纯锌与稀硫酸反应产生氢气的速率较慢,再加入少量CuSO4固体,反应速率加快 |
| A. | KOH | B. | MgCl2 | C. | CO2 | D. | CH4 |
①向KMnO4晶体中加入浓盐酸,产生的气体进行漂白实验后的尾气用NaOH溶液吸收;
②向Na2SO3晶体中滴入浓H2SO4,尾气用氨水吸收;
③向FeS固体中滴入稀盐酸,最后的尾气用CuSO4溶液吸收;
④浓H2SO4与食盐晶体共热,将多余的气体用水吸收.
| A. | ①④ | B. | ②③ | C. | ①③④ | D. | ①②③④ |
| A. | 将固体氢氧化钠用托盘天平直接称量 | |
| B. | 酒精灯的火焰必须用灯帽盖灭,不可用嘴吹灭 | |
| C. | 试管须用试管夹取用,且不能直接加热 | |
| D. | 用燃着的酒精灯去点燃另一个酒精灯 |
| A. | 金属钠 | B. | 氢氧化钠溶液 | C. | 盐酸 | D. | 溴水 |