题目内容
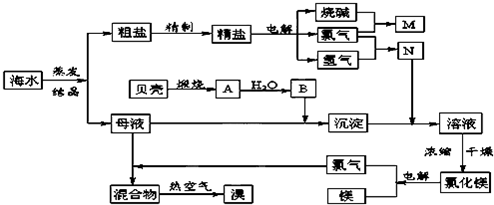
(8分)海水中含有丰富的化学元素,下面是某化工厂从海水中提取NaCl、Mg(以MgCl2形式存在)和Br2(以NaBr的形式存在)及综合利用的生产流程简图:
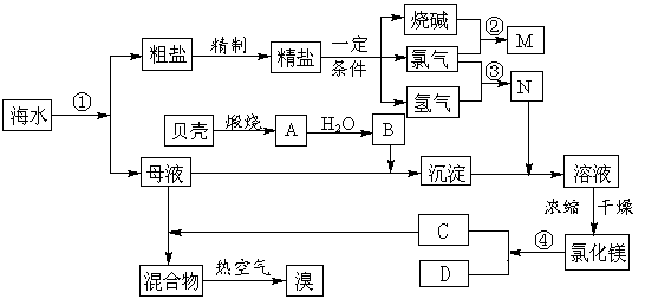
回答下列问题:
(1)流程图中操作①的名称为 。
(2)有同学认为:可直接加热Mg(OH)2得到MgO,再电解熔融的MgO制金属镁,这样可简化实验步骤,体现实验的简约性原则。你 (填“同意”或“不同意”)该同学的想法,理由是 ;
(3)该流程图里B、C反应可以生产工业上一重要产品,写出该反应的化学方程式:
(4)工业上从海水中提取的NaCl,可用来制取纯缄,其简要过程如下:向饱和食盐水中先通入气体X,后通入气体Y,充分反应后过滤得到晶体Z和滤液W,将晶体Z灼烧即可制得纯碱。已知气体X、Y是CO2或NH3,则气体X应是 (填化学式)。
(1)蒸发结晶 (2分)
(2)不同意 因为MgO熔点很高,熔融时耗费大量的能量而增加生产成本(每空1分)
(3)2Cl2+2Ca(OH)2 CaCl2+Ca(ClO)2+2H2O(2分)
(4)NH3(2分)

练习册系列答案
相关题目
 海水中含有丰富的化学元素,如图是某化工厂利用海水的生产镁的流程简图,请回答:
海水中含有丰富的化学元素,如图是某化工厂利用海水的生产镁的流程简图,请回答: