题目内容
【题目】将含有A、B、C三种离子的水溶液进行实验:

符合上述情况的三种金属离子
A.Ag+、Cu2+、Al3+
B.Ag+、Fe2+、Al3+
C.Ag+、Ba2+、Fe3+
D.Ag+、Cu2+、Fe3+
【答案】A
【解析】
向含有A+、B2+、C3+离子的溶液中加入足量的盐酸,A+离子生成了白色沉淀,可知A+离子为银离子;再向含有B2+、C3+离子的酸性溶液中加入H2S,生成了沉淀,该沉淀不溶于盐酸,该沉淀为CuS,B2+为Cu2+(H2S不能和Fe2+反应,因为FeS溶于稀盐酸),过滤后得到了C3+离子和沉淀,说明C3+不与H2S反应,C3+离子一定不是Fe3+;足量氨水与C3+反应生成沉淀,只能为铝Al3+,则溶液中含有Ag+、Cu2+、Al3+,故答案为A。

练习册系列答案
相关题目
【题目】下图是物质间发生化学反应的颜色变化,下表选项物质对应正确的是
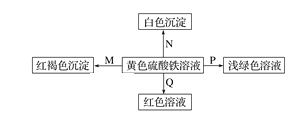
选项 | M | N | P | Q |
A | NH3·H2O | Ba(OH)2 | 铜 | KSCN |
B | Na | BaCl2 | FeO | KSCN |
C | NaOH | Ba(NO3)2 | 锌粉 | KSCN |
D | Na2O2 | MgCl2 | Fe | KSCN |
A.AB.BC.CD.D