题目内容
常温下,取0.3 mol/L HY溶液与0.3 mol/L NaOH溶液等体积混合(不计混合后溶液体积变化),测得混合溶液的pH=9,则下列说法(或关系式)正确的是
A.混合溶液中由水电离出来的c(OH-)=1×10-9 mol/L
B.混合溶液中离子浓度大小次序为:c(Y-)>c(Na+)>c(OH-)>c(H+)
C.c(OH-)=c(HY)=c(H+)=1×10-9 mol/L
D.c(Na+)=c(Y-)+c(HY)=0.3 mol/L
C
【解析】
试题分析:取0.3mol•L-1HY溶液与0.3mol•L-1NaOH溶液等体积混合,恰好反应生成NaY,测得混合溶液的pH=9,说明溶液呈碱性,这说明NaY为强碱弱酸盐,则A、NaY为强碱弱酸盐,水解呈碱性,水解促进水的电离,所以混合溶液中由水电离出的c(OH-)=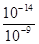 =mol/L=10-5mol/L,故A错误;B、溶液呈碱性,则有c(OH-)>c(H+),根据电荷守恒c(Na+)+c(H+)=c(Y-)+c(OH-),可得c(Na+)>c(Y-),溶液中离子浓度由大到小的顺序为 c(Na+)>c(Y-)>c(OH-)>c(H+),故B错误;C、根据物料守恒,应有c(HY)+c(Y-)=c(Na+),根据电荷守恒应有c(Na+)+c(H+)=c(Y-)+c(OH-),二者联式可得:c(HY)+c(H+)=c(OH-),则c(OH-)-c(HY)=c(H+)=1×10-9mol•L-1,故C正确;D、0.3mol•L-1HY溶液与0.3mol•L-1NaOH溶液等体积混合后,从物料守恒的角度分析,溶液中应存在c(Na+)=c(Y-)+c(HY)=0.15mol•L-1,故D错误,答案选C。
=mol/L=10-5mol/L,故A错误;B、溶液呈碱性,则有c(OH-)>c(H+),根据电荷守恒c(Na+)+c(H+)=c(Y-)+c(OH-),可得c(Na+)>c(Y-),溶液中离子浓度由大到小的顺序为 c(Na+)>c(Y-)>c(OH-)>c(H+),故B错误;C、根据物料守恒,应有c(HY)+c(Y-)=c(Na+),根据电荷守恒应有c(Na+)+c(H+)=c(Y-)+c(OH-),二者联式可得:c(HY)+c(H+)=c(OH-),则c(OH-)-c(HY)=c(H+)=1×10-9mol•L-1,故C正确;D、0.3mol•L-1HY溶液与0.3mol•L-1NaOH溶液等体积混合后,从物料守恒的角度分析,溶液中应存在c(Na+)=c(Y-)+c(HY)=0.15mol•L-1,故D错误,答案选C。
考点:考查酸碱中和滴定溶液酸碱性的判断;溶液pH计算以及溶液中离子浓度大小比较等

 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案Ⅱ.废旧金属的回收再利用是保护自然资源的有力措施.一批成分不详的合金废料,为了确定其成分和再利用途径,探究性学习小组拟定以下方案进行实验分析:
请回答下列问题:
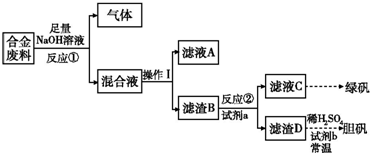
(1)从上述信息知,该合金中可确定的成分有
(2)滤渣D中加入稀硫酸和试剂b,常温下可制得胆矾,是一种绿色化学工艺,则试剂b是
(3)甲、乙两同学都验证了反应①生成气体是氢气,甲同学推断滤液A应是NaAlO2;乙同学查阅资料得知硅与NaOH溶液反应也有H2放出,因此持不同意见,请你设计一最佳方案,帮助他们作一确证:(写出选用试剂、实验判断现象及得出结论)
(4)取质量均为m g的滤渣B四份,分别加入同浓度,不同体积的稀HNO3充分反应,在标准状况生成NO(设还原产物只有一种)体积与剩余固体金属的质量如下表:
| 实验编号 | 1 | 2 | 3 | 4 |
| 稀HNO3体积(mL) | 100 | 200 | 300 | 400 |
| 剩余金属质量(g) | 9.0 | 4.8 | 0 | 0 |
| NO体积(L) | 1.12 | 2.24 | 3.36 | V |
②写出实验4中金属恰好溶解后,发生反应的离子方程式:
 (2012?成都模拟)溶液中的化学反应大多是离子反应.根据要求回答下列问题.
(2012?成都模拟)溶液中的化学反应大多是离子反应.根据要求回答下列问题.