题目内容
【题目】设NA为阿伏加德罗常数的数值,下列有关叙述正确的是 ( )
A.100 g 98%的浓硫酸中含有的氢原子数目为2NA
B.16g16O2和18O3的混合物中含有的质子数目为8NA
C.电解精炼铜的过程中,若阳极减重64g,则电路中一定通过2NA个电子
D.取50mL14.0mol/L浓硝酸与足量的铜片反应,生成气体分子的数目可能为0.25NA
【答案】D
【解析】
根据题中阿伏加德罗常数可知,本题考查阿伏加德罗常数的相关计算,运用![]() 分析。
分析。
A.浓硫酸中除了硫酸外,水也含H原子,故溶液中的H原子个数多于2NA个,A项错误;
B. 16O2和18O3的摩尔质量不同,且两者的比例未知,故16g混合物的物质得量无法计算,B项错误;
C.电解精炼铜时,阳极上放电的不只是铜,还有比铜活泼的金属,故当减轻64g时,阳极上失去的电子多于2NA个,C项错误;
D. 取50mL14.0moI/L浓硝酸与足量的铜片反应,开始生成的是NO2,随着硝酸变稀,生成的气体为NO、N2等,故生成的气体分子个数小于0.35NA个,故可能为0.25NA个,D项正确;
答案选D。

【题目】以SO2、软锰矿(主要成分MnO2,少量Fe、Al、Ca及Pb的化合物等)、氨水及净化剂等为原料可制备MnSO4溶液和Mn3O4,主要实验步骤如下:

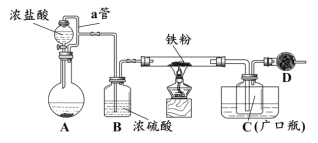
步骤Ⅰ:如图所示装置,将SO2通入B中的软锰矿浆液中(MnO2+SO2 = MnSO4)。
步骤Ⅱ:充分反应后,在不断搅拌下依次向三口烧瓶中加入适量纯净的MnO2、MnCO3,最后加入适量Na2S沉铅等重金属。
步骤Ⅲ:过滤得MnSO4溶液。
(1)装置A用于制取SO2,反应的化学方程式为_____。
(2)装置B中反应应控制在90~100℃,适宜的加热方式是_____。
(3)装置C的作用是_____。
(4)“步骤Ⅱ”中加入纯净MnO2的目的是_____,用MnCO3调节溶液pH时,需调节溶液pH范围为_____(该实验条件下,部分金属离子开始沉淀和沉淀完全的pH如下)。
金属离子 | Fe2+ | Fe3+ | Al3+ | Mn2+ |
开始沉淀pH | 7.04 | 1.87 | 3.32 | 7.56 |
沉淀完全pH | 9.18 | 3.27 | 4.9 | 10.2 |
(5)已知:①用空气氧化Mn(OH)2浊液可制备Mn3O4[6Mn(OH)2+O2![]() 2Mn3O4+6H2O],主要副产物为MnOOH;反应温度和溶液pH对产品中Mn的质量分数的影响如下图所示:
2Mn3O4+6H2O],主要副产物为MnOOH;反应温度和溶液pH对产品中Mn的质量分数的影响如下图所示:
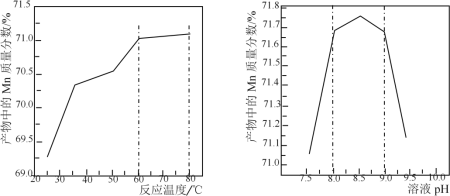
②反应温度超过80℃时,Mn3O4产率开始降低。
③Mn(OH)2是白色沉淀,Mn3O4呈黑色;Mn3O4、MnOOH中锰的质量分数理论值依次为72.03%、62.5%。
请补充完整由步骤Ⅲ得到的MnSO4溶液,并用氨水等制备较纯净的Mn3O4的实验方案:_____,真空干燥6小时得产品Mn3O4。