题目内容
6.下列说法或表示方法正确的是( )| A. | 若将等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 | |
| B. | 由“C(石墨)=C(金刚石)△H=+1.9 kJ•mol-1”可知,金刚石比石墨稳定 | |
| C. | 在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)═2H2O(l)△H=+285.8 kJ•mol-1 | |
| D. | 在稀溶液中:H++OH-═H2O△H=-57.3 kJ•mol-1,若将含1 mol CH3COOH与含1 mol NaOH的溶液混合,放出的热量小于57.3 kJ |
分析 A、硫单质从固体变为气体是一个吸热的过程;
B、物质具有的能量越低越稳定;
C、根据热化学方程式的意义:2gH2全燃烧生成液态水,放出285.8kJ热量;
D、醋酸电离吸热.
解答 解:A、硫单质从固体变为气体是一个吸热的过程,所以将等量的硫蒸气和硫固体分别完全燃烧,前者放出热量多,故A错误;
B、由“C(石墨)═C(金刚石)△H=+1.9kJ/mol”可知石墨的能量低于金刚石,所以石墨比金刚石稳定,故B错误;
C、101 kPa时,2gH2 完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ•mol-1,故C错误;
D、在稀溶液中:H++OH-═H2O△H=-57.3 kJ•mol,若将含1 mol CH3COOH与含1 mol NaOH的溶液混合,由于醋酸电离时吸热,所以放出的热量小于57.3kJ,故D正确.
故选D.
点评 本题考查反应中能量变化、热化学方程式、反应进行方向判断,难度不大,注意热化学方程式书写,侧重于考查学生对基础知识的掌握情况.

练习册系列答案
相关题目
17.填下列表格
| 物质 | 分子数 | 质量/g | 物质的量/mol | 摩尔质量/g.mol-1 |
| O2 | 8.0 | |||
| H2SO4 | 3.01×1023 |
14.某兴趣小组的同学用如图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转.一段时间后,断开电键K,下列物质能使乙池恢复到反应前浓度的是( )
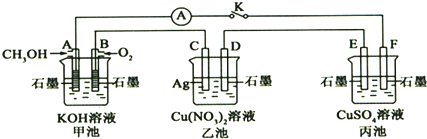

| A. | Cu | B. | CuO | C. | Cu(OH)2 | D. | Cu2(OH)2CO3 |
18.下列判断中一定正确的是( )
| A. | 若 R2-和 M+的电子层结构相同,则原子序数:M>R | |
| B. | 若 X、Y是同主族气态氢化物,且相对分子质量:X>Y,则沸点:X>Y | |
| C. | 若 M、N是同主族非金属元素,且电子层数:M>N,则非金属性:M>N | |
| D. | 若 X、Y属于同周期元素,且原子序数:X>Y,则最高正价:X>Y |
 2NH3;
2NH3;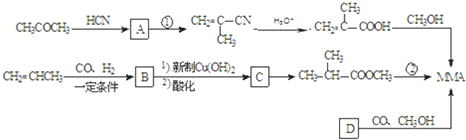
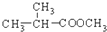 互为同分异构体,则其物质结构简式为HCOOCH(CH3)CH2CH3
互为同分异构体,则其物质结构简式为HCOOCH(CH3)CH2CH3 +CH3CH2CH2OH→
+CH3CH2CH2OH→ +CH3OH
+CH3OH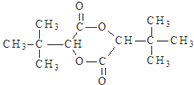 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
的合成路线流程图(无机试剂任选).合成路线流程图示例如下: