题目内容
【题目】下列各组变化中,化学反应的反应热前者大于后者的一组是( )
①CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H1; CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H2;
②2H2(g)+O2(g)=2H2O(l)△H1; H2(g)+O2(g)=H2O(l)△H2
③t℃时,在一定条件下,将1molSO2和1molO2混合后,分别置于恒容和恒压的两个密闭容器中,达到平衡状态时放出的热量分别为Q1、Q2
④CaCO3(s)=CaO(s)+CO2(g)△H1;CaO(s)+H2O(l)=Ca(OH)2(s)△H2
A. ①③④ B. ②③ C. ①④ D. ①②④
【答案】C
【解析】①水蒸气转化成液态水,是放热过程,即△H1>△H2,故①正确;②△H1=2△H2,因为氢气燃烧是放热反应,即△H1<△H2,故②错误;③2SO2(g)+O2(g)![]() 2SO3(g) △H<0,恒压状态下,SO2的转化率大于恒容时的转化率,因此有Q1<Q2,故③错误;④CaCO3分解是吸热反应,即△H1>0,CaO与水反应是放热反应,即△H2<0,因此有△H1>△H2,故④正确;综上所述,选项C正确。
2SO3(g) △H<0,恒压状态下,SO2的转化率大于恒容时的转化率,因此有Q1<Q2,故③错误;④CaCO3分解是吸热反应,即△H1>0,CaO与水反应是放热反应,即△H2<0,因此有△H1>△H2,故④正确;综上所述,选项C正确。

【题目】在一定条件下,将燃煤废气中的CO2转化为二甲醚的反应为:2CO2(g)+6H2(g)![]() CH3OCH3(g+3H2(g) △H
CH3OCH3(g+3H2(g) △H
已知:①CO(g)+2H2(g)![]() CH3OH(g) △H1=-90.7kJ.mol-l
CH3OH(g) △H1=-90.7kJ.mol-l
②2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H2=-23.5kJ.mol-l
CH3OCH3(g)+H2O(g) △H2=-23.5kJ.mol-l
③CO(g)+H2O(g)![]() CO2(g)+H2(g) △H2=-41.2kJ.mol-l
CO2(g)+H2(g) △H2=-41.2kJ.mol-l
(1)△H_____ kJ.mol-l
(2)某温度下,在体积固定为2L的密闭容器中进行反应①,将1molCO和2molH2混合,测得不同时刻的反应前后压强关系如下:
时间(min) | 5 | 10 | 15 | 20 | 25 | 30 |
压强比(P前/P后) | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
则达到平衡时CO的转化率为_________。
(3)已知在某压强下,该反应在不同温度、不同投料比[n(H2)/n(CO2)]时,CO2的转化率如右图所示。从图中可得出三条主要规律:
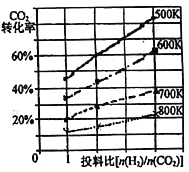
①增大投料比,CO2的转化率增大;②_____________;③_______________。
(4)反应③的v-t图像如图1所示,若其他条件不变,只是在反应前增大容器体积使压强减小,则其v-t图像如图2所示。
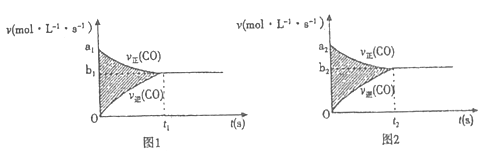
下列说法正确的是________。
①a1>a2 ②a1<a2 ③b1>b2 ④b1<b2 ⑤t1>t2 ⑥t1=t2 ⑦ t1<t2 ⑧两图中阴影部分面积相等⑨右图阴影部分面积更大 ⑩左图阴影部分面积更大
A. ①③⑦⑧ B. ①③⑤⑧ C. ②④⑦⑨ D. ①③⑦⑩
(5)由甲醇液相脱水法也可制二甲醚,首先将甲醇与浓硫酸反应生成硫酸氢甲酯(CH3OSO3H):CH3OH+H2SO4→CH3OSO3H+H2O;生成的硫酸氢甲酯再和甲醇反应生成二甲醚,第二步的反应方程式为:____________。与CO2和H2反应制备二甲醚比较,该工艺的优点是反应温度低,转化率高,其缺点是______________。