题目内容
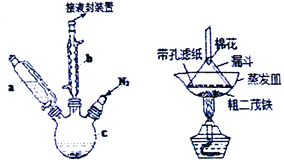
【题目】二茂铁可用作燃料的节能消烟剂、抗爆剂等。实验室制备二茂铁装置示意图如右下图(二茂铁熔点是173℃,在100℃时开始开华;沸点是249℃)。实验步骤为:
①在三颈烧瓶中加入25g粉末状的KOH,并从仪器a中加入60mL无水乙醚到烧瓶中,充分搅拌,同时通氮气约10min;
②再从仪器a滴入5.5mL新蒸馏的环戊二烯(密度0.95g/cm3),搅拌;
③将6.5g无水FeCl2与(CH3)2SO(二甲亚砜,作溶剂)配成的溶液25mL装入仪器a中,慢慢滴入仪器c中,45min滴完,继续搅拌45min;
④再从仪器a加入25mL无水乙醚搅拌;
⑤将c中的液体转入仪器d,依次用盐酸、水各洗涤两次,分液得橙黄色溶液;
⑥蒸发橙黄色溶液,得二茂铁粗产品。
回答下列问题:
(1)仪器b的名称是______________,作用是________________________。
(2)步骤①中通入氮气的目的是__________________________________。
(3)仪器c的适宜容积应为_________:①100mL、②250mL、③500mL;仪器a使用前应进行的操作是_______________________________________。
(4)KOH、FeCl2、C5H6反应生成二茂铁[Fe(C5H5)2]和KCl的化学方程式为_________________________;步骤⑦是二茂铁粗产品的提纯,该过程在右图中进行,其操作名称为 ____________________________。
(5)为了确证得到的是二茂铁,还需要进行的一项简单实验是_________________________。
(6)最终得到纯净的二茂铁3.7g,则该实验的产率为 __________________(保留两位有效数字)。
【答案】 球形冷凝管 冷凝回流有机物(或乙醚、环戊二烯和二甲亚砜) 将装置中的空气排尽(或排尽。除去氧气),防止(避免、不让)实验过程中Fe2+被氧化 ② 检漏或检查是否漏水 2KOH+FeCl2+2C5H6=Fe(C5H5)2+2KCl+2H2O 升华 测定所得固体的熔点 50%
【解析】(1)根据装置图,仪器b为冷凝管,可以冷凝回流有机物(或乙醚、环戊二烯和二甲亚砜),故答案为:冷凝管;冷凝回流有机物;
(2)二茂铁中铁是+2价,易被空气中氧气氧化,步骤①中通入氮气排尽装置中空气,防止实验过程中亚铁离子被氧化,故答案为:排尽装置中空气,防止实验过程中亚铁离子被氧化;
(3)由题意可知三颈烧瓶中共加入液体110mL,三颈烧瓶中盛放液体的体积不超过容积的![]() ,所以选择250mL,故选②,仪器a为恒压漏斗,使用前需要检查是否滤液,故答案为:②;检漏;
,所以选择250mL,故选②,仪器a为恒压漏斗,使用前需要检查是否滤液,故答案为:②;检漏;
(4)KOH、FeCl2、C5H6反应生成二茂铁[Fe(C5H5)2]和KCl的化学方程式为2KOH+FeCl2+2C5H6=Fe(C5H5)2+2KCl+2H2O;二茂铁有固体直接变成气体,然后冷凝收集,其操作名称为升华,故答案为:2KOH+FeCl2+2C5H6=Fe(C5H5)2+2KCl+2H2O;升华;
(5)为了确证得到的是二茂铁,还需要进行的一项简单实验是测定所得固体的熔点;故答案为:测定所得固体的熔点;
(6)二茂铁的理论产量为![]() ×
×![]() ×186g/mol=7.4g,则产率=
×186g/mol=7.4g,则产率=![]() ×100%=50%;故答案为:50%。
×100%=50%;故答案为:50%。