题目内容
(8分)Cu—Fe合金由于长时间置于空气中,表面产生了一层氧化膜(成份为Fe2O3和CuO),现进行如下实验(以下气体体积均在标况下测得):
①将此合金块5.76g置于烧杯中,然后将稀H2SO4逐渐缓慢加入至过量,收集产生的气体为672mL,过滤得浅绿色溶液A,还有滤渣B。
②将滤渣B投入到一定浓度的HNO3中,完全溶解,得NO、NO2的混合气体896mL,经测定,同温同压下此混合气体对氢气的相对密度为17。
③将①中所得滤液加入到同浓度足量的HNO3中,用排水法收集一烧瓶气体,再向烧瓶中通入224mL O2,气体恰好完全溶于水。
(1)A中存在的阳离子有 ;
(2)896mL混合气体中NO、NO2的物质的量之比为 ;
(3)B的单质为 ,质量为 g;
(4)③中被HNO3氧化了的阳离子的物质的量为 mol;
(5)此合金块中氧元素的质量为 g。
①将此合金块5.76g置于烧杯中,然后将稀H2SO4逐渐缓慢加入至过量,收集产生的气体为672mL,过滤得浅绿色溶液A,还有滤渣B。
②将滤渣B投入到一定浓度的HNO3中,完全溶解,得NO、NO2的混合气体896mL,经测定,同温同压下此混合气体对氢气的相对密度为17。
③将①中所得滤液加入到同浓度足量的HNO3中,用排水法收集一烧瓶气体,再向烧瓶中通入224mL O2,气体恰好完全溶于水。
(1)A中存在的阳离子有 ;
(2)896mL混合气体中NO、NO2的物质的量之比为 ;
(3)B的单质为 ,质量为 g;
(4)③中被HNO3氧化了的阳离子的物质的量为 mol;
(5)此合金块中氧元素的质量为 g。
(共8分)
(1)Fe2+、H+ 1分)
(2)3:1(1分)
(3)Cu (1分) 3.2 g(1分)
(4)0.04 mol (2分)(5)0.32(2分)
(1)Fe2+、H+ 1分)
(2)3:1(1分)
(3)Cu (1分) 3.2 g(1分)
(4)0.04 mol (2分)(5)0.32(2分)
略

练习册系列答案
相关题目
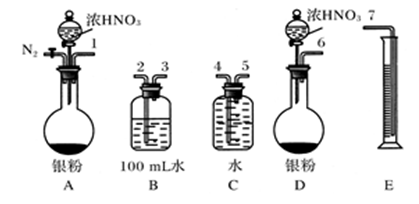
 实验方案验证Ag与浓HNO3反应的
实验方案验证Ag与浓HNO3反应的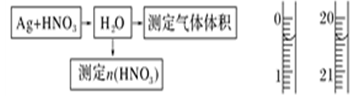
 液,用0.1 mol·L-1的NaOH溶液滴定,用酚酞作指示剂,滴定前后的滴定管中液面的位置
液,用0.1 mol·L-1的NaOH溶液滴定,用酚酞作指示剂,滴定前后的滴定管中液面的位置 如上图所示。在B容器中生成硝酸的物质的量为__
如上图所示。在B容器中生成硝酸的物质的量为__