题目内容
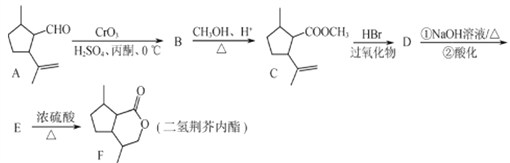
【题目】下列对浓硫酸的叙述正确的是
A. 常温下,浓硫酸与铁、铝不反应
B. 浓硫酸具有吸水性,故能使蔗糖炭化
C. 浓硫酸可作H2、NH3等气体的干燥剂,表现脱水性
D. 浓硫酸和铜片加热时发生反应,表现酸性和氧化性
【答案】D
【解析】
A.常温下浓硫酸与铁、铝发生钝化,在铁、铝表面形成一薄层致密氧化膜阻止反应进行,故A错误;
B.浓硫酸使蔗糖炭化体现其脱水性,故B错误;
C.浓硫酸不能干燥NH3,浓硫酸可作H2的干燥剂体现其吸水性,故C错误;
D.浓硫酸和铜片加热时发生反应生成硫酸铜表现酸性,生成二氧化硫,硫元素化合价由+6价变化为+4价,表现氧化性,故D正确;
故选D。

练习册系列答案
相关题目
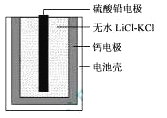
【题目】实验室模拟电解法处理含六价铬的工业废水,用如图装置将主要有害物Cr2O72-转化为Cr3+(无害)除去。得到如下实验结果:

实验 | 实验条件 | Cr2O72- |
① | A电极为石墨 | 0.922% |
② | A电极为石墨,废水中加入1mL浓硫酸 | 12.7% |
③ | A电极为铁,废水中加入1mL浓硫酸 | 57.3% |
下列说法中,正确的是
A. 对比实验①②可知,升高pH可以提高Cr2O72-的去除率
B. 实验②中, Cr2O72-在阳极放电,电极反应式为Cr2O72-+6e-+14H+=2Cr3++7H2O
C. 对比实验②③可知, Cr2O72-去除率增大的原因是A电极产生的Fe2+也能还原Cr2O72-
D. 实验③中,理论上电路中每通过6mol电子,则有1mol Cr2O72-被还原