题目内容
【题目】25℃时,用NaOH溶液滴定H2C2O4溶液,溶液中-1g[c(H+)/c(H2C2O4)]和-1gc(HC2O4-)或-1g[c(H+)/c(HC2O4-)]和-1gc(C2O42-)关系如图所示,下列说法不正确的是
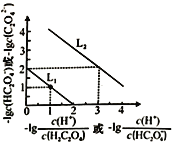
A. 曲线L1表示-1g[c(H+)/c(H2C2O4)]和-1gc(HC2O4-)的关系
B. Ka2(H2C2O4)的数量级为10-2
C. 已知 NaHC2O4溶液的pH<7,则溶液中c(Na+)>c(HC2O4-)>c(C2O42-)>c(H2C2O4)
D. 向0.1mol/L H2C2O4溶液中加入少量水[c(HC2O4-)/c(H2C2O4)]增大
【答案】B
【解析】A.H2CO4为弱酸,第一步电离平衡常数>第二步电离平衡常数,即![]() 则
则![]() 则
则![]() ,因此曲线L1表示-1g[c(H+)/c(H2C2O4)]和-1gc(HC2O4-)的关系,曲线L2表示-1g[c(H+)c(HC2O4)和-1gc(C2O42-)的关系,故A正确;B.根据上述分析,因为
,因此曲线L1表示-1g[c(H+)/c(H2C2O4)]和-1gc(HC2O4-)的关系,曲线L2表示-1g[c(H+)c(HC2O4)和-1gc(C2O42-)的关系,故A正确;B.根据上述分析,因为![]() ,则
,则![]() ,故B错误;C.根据B的分析,Ka1(H2C2O4)=10-2,则NaHC2O4的水解平衡常数
,故B错误;C.根据B的分析,Ka1(H2C2O4)=10-2,则NaHC2O4的水解平衡常数![]() ,说明以电离为主,溶液显酸性,则c(Na+)>c(HC2O4-)>c(C2O42-)>c(H2C2O4),故C正确;D.向0.1mol/L H2C2O4溶液中加入少量水,草酸的电离程度增大,[c(HC2O4-)/c(H2C2O4)]增大,故D正确;本题选B。
,说明以电离为主,溶液显酸性,则c(Na+)>c(HC2O4-)>c(C2O42-)>c(H2C2O4),故C正确;D.向0.1mol/L H2C2O4溶液中加入少量水,草酸的电离程度增大,[c(HC2O4-)/c(H2C2O4)]增大,故D正确;本题选B。

练习册系列答案
相关题目