题目内容
在容积一定的密闭容器中,置入一定量的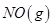 和足量
和足量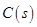 ,发生反应
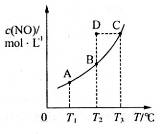
,发生反应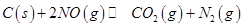 ,平衡状态时NO(g)的物质的量浓度c(NO)与温度T的关系如图所示,则下列说法中,正确的是
,平衡状态时NO(g)的物质的量浓度c(NO)与温度T的关系如图所示,则下列说法中,正确的是
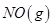 和足量
和足量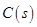 ,发生反应
,发生反应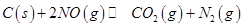 ,平衡状态时NO(g)的物质的量浓度c(NO)与温度T的关系如图所示,则下列说法中,正确的是
,平衡状态时NO(g)的物质的量浓度c(NO)与温度T的关系如图所示,则下列说法中,正确的是
| A.该反应的△H>0 |
B.若该反应在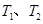 时的平衡常数分别为 时的平衡常数分别为 ,则 ,则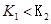 |
C.在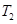 时,若反应体系处于状态D,则这时一定有 时,若反应体系处于状态D,则这时一定有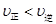 |
D.在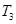 时,若混合气体的密度不再变化,则可以判断反应达到平衡状态 时,若混合气体的密度不再变化,则可以判断反应达到平衡状态 |
D
试题分析:A、随着温度的升高,反应物NO的浓度增大,平衡向左移动,说明该反应为放热反应,?H<0,错误;B、因为该反应为放热反应,T2>T1,则K1 > K2,错误;C、在T2时,若反应体系处于状态D,因为D在平衡曲线的上方,所以一定有v正>v逆,错误;D、因为C为固态,所以反应向左或向右进行,混合气体的密度发生变化,所以若混合气体的密度不再变化,则可以判断反应达到平衡状态,正确。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 B(g)+C(g)达到平衡后,升高温度容器内气体的密度增大,则下列叙述正确的是 ( )
B(g)+C(g)达到平衡后,升高温度容器内气体的密度增大,则下列叙述正确的是 ( ) CH3OH(g)△H1=-116 kJ·mol-1
CH3OH(g)△H1=-116 kJ·mol-1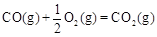 △H2=-283 kJ·mol-1
△H2=-283 kJ·mol-1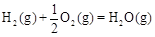 △H3=-242 kJ·mol-1
△H3=-242 kJ·mol-1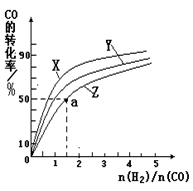
 2BaO(s)+O2(g)达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是
2BaO(s)+O2(g)达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是
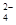
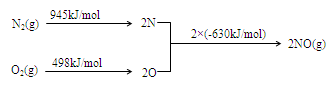
 2NO(g)△H= 。
2NO(g)△H= 。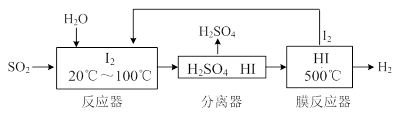
 NiO(OH)+MH,电池放电时,负极电极反应式为 ; 充电完成时,全部转化为NiO(OH),若继续充电,将在一个电极产生O2,O2扩散到另一个电极发生电极反应被消耗,从而避免产生的气体引起电池爆炸。
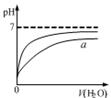
NiO(OH)+MH,电池放电时,负极电极反应式为 ; 充电完成时,全部转化为NiO(OH),若继续充电,将在一个电极产生O2,O2扩散到另一个电极发生电极反应被消耗,从而避免产生的气体引起电池爆炸。 Cr2O72- + H2O, K=1×1014。若用0.05mol K2Cr2O7配制成1 L K2CrO4溶液,其中c(Cr2O72-)<10-5mol/L,则所配溶液的pH
Cr2O72- + H2O, K=1×1014。若用0.05mol K2Cr2O7配制成1 L K2CrO4溶液,其中c(Cr2O72-)<10-5mol/L,则所配溶液的pH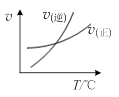
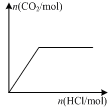

 CH3OH(g)+H2O(g)△H<0,若将6mo1 CO2和8mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化的曲线如右图所示(实线)。
CH3OH(g)+H2O(g)△H<0,若将6mo1 CO2和8mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化的曲线如右图所示(实线)。
