题目内容
(2010?启东市模拟)随着纳米材料在生产生活和科学研究中越来越广泛的应用,很多同学对其产生了浓厚的兴趣和探究的欲望.某化学学习小组通过查阅有关资料,按下列步骤自己动手制备纳米铁粉.请结合实验操作回答相关问题.
(1)草酸亚铁晶体(FeC2O4?2H2O)的制备

①现有烧杯、玻璃棒、药匙、滤纸、托盘天平、胶头滴管等实验仪器,为配制上述两种溶液,缺少的玻璃仪器为
②过滤、洗涤过程中,检验草酸亚铁晶体是否洗净的方法是
③分析上述草酸亚铁晶体的制备方案,可推FeC2O4?2H2O具备的性质是
a.在水中溶解度较小 b.不稳定,受热易分解
c.白色固体 d.易被空气氧化
(2)纳米铁粉的制备
将一根长度约为12cm~14cm的玻璃管在酒精喷灯上烧制成如图所示形状,向其中加入黄色草酸亚铁晶体.再将管口部分加热拉细,然后在酒精喷灯上均匀加热.当草酸亚铁粉末受热完全变黑,立即将管口拉细的部分放在火焰烧熔封闭, 这样便得到了高纯度的纳米铁粉.
这样便得到了高纯度的纳米铁粉.
①制备纳米铁粉,反应的化学方程式为
②实验前无需排尽装置中的空气,原因是
(1)草酸亚铁晶体(FeC2O4?2H2O)的制备

①现有烧杯、玻璃棒、药匙、滤纸、托盘天平、胶头滴管等实验仪器,为配制上述两种溶液,缺少的玻璃仪器为
500mL容量瓶
500mL容量瓶
,需称量FeSO4?7H2O的质量为34.8
34.8
g.②过滤、洗涤过程中,检验草酸亚铁晶体是否洗净的方法是
取最后的洗涤液,测定洗涤液的pH,若洗涤液的pH等于7,说明已经洗涤干净(或取最后的洗涤液,向其中滴加BaCl2溶液,若无浑浊产生,则说明已经洗涤干净)
取最后的洗涤液,测定洗涤液的pH,若洗涤液的pH等于7,说明已经洗涤干净(或取最后的洗涤液,向其中滴加BaCl2溶液,若无浑浊产生,则说明已经洗涤干净)
.③分析上述草酸亚铁晶体的制备方案,可推FeC2O4?2H2O具备的性质是
ab
ab
.a.在水中溶解度较小 b.不稳定,受热易分解
c.白色固体 d.易被空气氧化
(2)纳米铁粉的制备
将一根长度约为12cm~14cm的玻璃管在酒精喷灯上烧制成如图所示形状,向其中加入黄色草酸亚铁晶体.再将管口部分加热拉细,然后在酒精喷灯上均匀加热.当草酸亚铁粉末受热完全变黑,立即将管口拉细的部分放在火焰烧熔封闭,
 这样便得到了高纯度的纳米铁粉.
这样便得到了高纯度的纳米铁粉.①制备纳米铁粉,反应的化学方程式为
FeC2O4?2H2O
Fe+2CO2↑+2H2O↑
| ||
FeC2O4?2H2O
Fe+2CO2↑+2H2O↑
.
| ||
②实验前无需排尽装置中的空气,原因是
反应生成CO2驱赶装置中空气,防止红热的铁被氧化
反应生成CO2驱赶装置中空气,防止红热的铁被氧化
.分析:(1)①根据配制一定物质的量浓度的溶液步骤选择仪器;根据硫酸亚铁的浓度和体积计算出物质的量,再计算出需称量FeSO4?7H2O的质量;
②可以通过测定洗涤液的pH判断是否洗涤干净,也可以通过检验硫酸根离子判断洗涤情况;
③根据草酸亚铁晶体(FeC2O4?2H2O)的制备流程信息进行判断;
(2)①根据题中信息,醋酸亚铁晶体高温分解生成了铁粉,根据化合价变化写出反应方程式;
②根据反应方程式进行分析.
②可以通过测定洗涤液的pH判断是否洗涤干净,也可以通过检验硫酸根离子判断洗涤情况;
③根据草酸亚铁晶体(FeC2O4?2H2O)的制备流程信息进行判断;
(2)①根据题中信息,醋酸亚铁晶体高温分解生成了铁粉,根据化合价变化写出反应方程式;
②根据反应方程式进行分析.
解答:解:(1)①配制一定物质的量浓度的溶液步骤为:计算、称量、溶解、转移、洗涤、定容、摇匀等,需要的仪器有:烧杯、玻璃棒、药匙、滤纸、托盘天平、胶头滴管和容量瓶,所以还需要250mL容量瓶;需要硫酸亚铁的物质的量为:0.5mol/L×0.25L=0.125mol,需要FeSO4?7H2O的质量为:278g/mol×0.125mol=34.75g,需要托盘天平称量的质量是:34.8g,
故答案为:250mL容量瓶; 34.8;
②若是已经洗涤干净,洗涤液的pH应该等于7,所以可通过测定洗涤液的pH判断是否洗涤干净,方法为:取最后的洗涤液,测定洗涤液的pH,若洗涤液的pH等于7,说明已经洗涤干净(或取最后的洗涤液,向其中滴加BaCl2溶液,若无浑浊产生,则说明已经洗涤干净),
故答案为:取最后的洗涤液,测定洗涤液的pH,若洗涤液的pH等于7,说明已经洗涤干净(或取最后的洗涤液,向其中滴加BaCl2溶液,若无浑浊产生,则说明已经洗涤干净);
③根据制备流程,通过过滤获得草酸亚铁晶体,说明草酸亚铁的溶解度较小;所得的沉淀在烘箱中50℃以下烘干,说明温度高了草酸亚铁容易分解,但是不会被氧气氧化,所以正确的是a、b,
故选ab;
(2)①利用草酸亚铁晶体高温下制备纳米铁粉,草酸亚铁晶体中C的化合价是+3价,铁被还原,碳原子只能被氧化,生成了二氧化碳,反应的方程式为:FeC2O4?2H2O
Fe+2CO2↑+2H2O↑,
故答案为:FeC2O4?2H2O
Fe+2CO2↑+2H2O↑;
②该反应中,FeC2O4?2H2O
Fe+2CO2↑+2H2O↑,生成了二氧化碳,二氧化碳能够将空气赶走,防止了铁被氧化,
故答案为:反应生成CO2驱赶装置中空气,防止红热的铁被氧化.
故答案为:250mL容量瓶; 34.8;
②若是已经洗涤干净,洗涤液的pH应该等于7,所以可通过测定洗涤液的pH判断是否洗涤干净,方法为:取最后的洗涤液,测定洗涤液的pH,若洗涤液的pH等于7,说明已经洗涤干净(或取最后的洗涤液,向其中滴加BaCl2溶液,若无浑浊产生,则说明已经洗涤干净),
故答案为:取最后的洗涤液,测定洗涤液的pH,若洗涤液的pH等于7,说明已经洗涤干净(或取最后的洗涤液,向其中滴加BaCl2溶液,若无浑浊产生,则说明已经洗涤干净);
③根据制备流程,通过过滤获得草酸亚铁晶体,说明草酸亚铁的溶解度较小;所得的沉淀在烘箱中50℃以下烘干,说明温度高了草酸亚铁容易分解,但是不会被氧气氧化,所以正确的是a、b,
故选ab;
(2)①利用草酸亚铁晶体高温下制备纳米铁粉,草酸亚铁晶体中C的化合价是+3价,铁被还原,碳原子只能被氧化,生成了二氧化碳,反应的方程式为:FeC2O4?2H2O
| ||
故答案为:FeC2O4?2H2O
| ||
②该反应中,FeC2O4?2H2O
| ||
故答案为:反应生成CO2驱赶装置中空气,防止红热的铁被氧化.
点评:本题考查了草酸亚铁晶体(FeC2O4?2H2O)和纳米铁粉的制备,涉及了一定物质的量浓度的溶液配制方法及仪器选择、根据信息推断物质的性质、化学方程式的书写等知识,题量较大,特别是书写草酸亚铁晶体的分解方程式,需要根据化合价判断产物二氧化碳,本题难度中等.

练习册系列答案
相关题目
 (R1、R2、R3代表烃基)
(R1、R2、R3代表烃基)

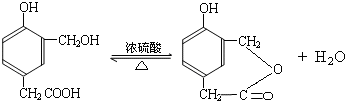
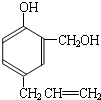
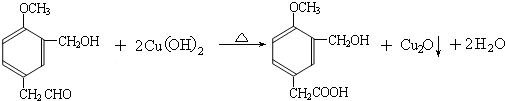
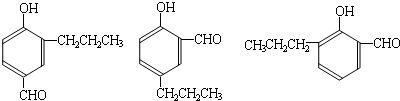
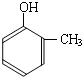 到的合成
到的合成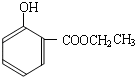 路线(用合成路线流程图表示,并注明反应条件).
路线(用合成路线流程图表示,并注明反应条件).
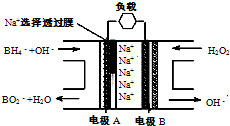 (2010?启东市模拟)直接NaBH4/H2O2燃料电池(DBFC)的结构如图,“负极材料采用Pt/C,正极材料采用MnO2”,有关该电池的说法正确的是
(2010?启东市模拟)直接NaBH4/H2O2燃料电池(DBFC)的结构如图,“负极材料采用Pt/C,正极材料采用MnO2”,有关该电池的说法正确的是