题目内容
9.如表实验方案设计中,不能达到实验目的是( )| 选项 | 实验目的 | 实验方案 |
| A | 验证乙烯与溴发生加成反应 | 乙烯通入溴水中,测定反应前后溶液pH |
| B | 检验氯化铁溶液中是否含FeCl2 | 向氯化铁溶液中滴加铁氰化钾溶液 |
| C | 检验乙酸中是否混有乙醇 | 取样液于试管,加入一绿豆颗粒大的钠粒 |
| D | 验证Ksp(AgI)<Ksp(AgCl) | 向含等物质的量NaCl、KI的混合液中滴加AgNO3溶液 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.加成反应后,酸性不明显,而发生取代反应生成HBr,酸性增强;
B.滴加铁氰化钾溶液,与亚铁离子反应产生蓝色沉淀;
C.乙酸、乙醇均与Na反应生成氢气;
D.先生成沉淀的溶度积小.
解答 解:A.若发生加成反应,溶液酸性变化不明显;若发生取代反应,溶液酸性增强,测定反应前后溶液pH,可验证乙烯与溴发生加成反应,故A正确;
B.滴加铁氰化钾溶液,产生蓝色沉淀说明含有FeCl2,故B正确;
C.乙酸、乙醇均能与钠反应产生气体,不能检验是否含乙醇,故C错误;
D.先产生黄色沉淀,证明Ksp(AgI)<Ksp(AgCl),能达到实验目的,故D正确;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及有机物的性质、离子检验、沉淀的生成等,把握物质的性质、反应原理为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案
相关题目
17.一定条件下,在容积固定不变的密闭容器中加入一定量的X和Y进行如下可逆反应,2X(g)+Y(s)?Z(g)+W(g)△H>0,一段时间后达到化学平衡状态后,再改变某一条件,下列有关叙述正确的是( )
| A. | 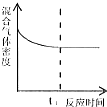 t1时刻表示该可逆反应达到新的平衡 | |
| B. |  横坐标x可表示温度或容器的体积 | |
| C. | 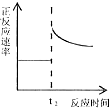 t2时刻改变的体积为加入少量的Y | |
| D. |  横坐标可表示为Z的体积分数 |
4.下列反应的离子方程式正确的是( )
| A. | 碳酸钠的水解反应 CO32-+H2O→HCO3-+OH - | |
| B. | 碳酸氢钙与过量的NaOH溶液反应Ca2++2HCO3-+2OH-→CaCO3↓+2H2O+CO32- | |
| C. | 苯酚钠溶液与二氧化碳反应 C6H5O-+CO2+H2O→C6H5OH+CO32- | |
| D. | 稀硝酸与过量的铁屑反应 3Fe+8H++2NO3-→3Fe3++2NO↑+4 H2O |
14.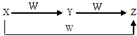 X、Y、Z、W有如图所示的转化关系,则X、Y可能是( )
X、Y、Z、W有如图所示的转化关系,则X、Y可能是( )
①C、CO ②S、SO2 ③AlCl3、Al(OH)3 ④Cl2、FeCl3.
 X、Y、Z、W有如图所示的转化关系,则X、Y可能是( )
X、Y、Z、W有如图所示的转化关系,则X、Y可能是( )①C、CO ②S、SO2 ③AlCl3、Al(OH)3 ④Cl2、FeCl3.
| A. | 仅有①③ | B. | ①②③ | C. | 仅有②④ | D. | ①②③④ |
19.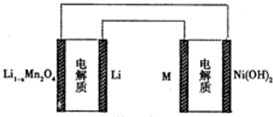 某充电宝锂离子电池的总反应为:xLi+Li1-nMn2O4$?_{充电}^{放电}$LiMn2O4,某手机镍氢电池总反应为:NiOOH+MH$?_{充电}^{放电}$M+Ni(OH)2(M为储氢金属或合金),有关上述 两种电池的说法不正确的是
某充电宝锂离子电池的总反应为:xLi+Li1-nMn2O4$?_{充电}^{放电}$LiMn2O4,某手机镍氢电池总反应为:NiOOH+MH$?_{充电}^{放电}$M+Ni(OH)2(M为储氢金属或合金),有关上述 两种电池的说法不正确的是
( )
 某充电宝锂离子电池的总反应为:xLi+Li1-nMn2O4$?_{充电}^{放电}$LiMn2O4,某手机镍氢电池总反应为:NiOOH+MH$?_{充电}^{放电}$M+Ni(OH)2(M为储氢金属或合金),有关上述 两种电池的说法不正确的是
某充电宝锂离子电池的总反应为:xLi+Li1-nMn2O4$?_{充电}^{放电}$LiMn2O4,某手机镍氢电池总反应为:NiOOH+MH$?_{充电}^{放电}$M+Ni(OH)2(M为储氢金属或合金),有关上述 两种电池的说法不正确的是( )
| A. | 锂离子电池放电时Li+向正极迁移 | |
| B. | 锂离子电池充电时,阴极的电极反应式:LiMn2O4-xe-=Li1-nMn2O4+xLi+ | |
| C. | 如图表示用锂离子电池给镍氢电池充电 | |
| D. | 镍氢电池放电时,正极的电极反应式:NiOOH+H2O+e-=Ni(OH)2+OH- |
16.已知:W是组成信息高速公路骨架的元素之一,且X、Y、Z、W在元素周期表中的位置如图所示.下列说法正确的是( )
| X | Y | |
| Z | W |
| A. | 最高正化合价:Z>X=W>Y | |
| B. | 原子半径:Y>X>W>Z | |
| C. | 最高价氧化物对应水化物的酸性:Z<X<W<Y | |
| D. | 最高价含氧酸的钠盐溶液能与SO2反应的:X、Y、Z、W |
16.下列说法不正确的是( )
| A. | 含氟氯代烃的废弃发泡塑料对臭氧层无影响 | |
| B. | 煤的气化是高效且清洁地利用煤炭的重要途径 | |
| C. | 将聚乙烯塑料经热裂解可得重新利用的小分子 | |
| D. | 使用无磷洗衣粉可缓解水体富营养化的趋势 |