题目内容
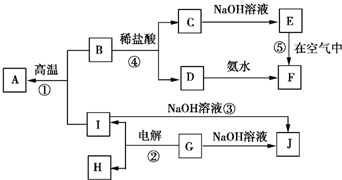
16.已知:W是组成信息高速公路骨架的元素之一,且X、Y、Z、W在元素周期表中的位置如图所示.下列说法正确的是( )| X | Y | |
| Z | W |
| A. | 最高正化合价:Z>X=W>Y | |
| B. | 原子半径:Y>X>W>Z | |
| C. | 最高价氧化物对应水化物的酸性:Z<X<W<Y | |
| D. | 最高价含氧酸的钠盐溶液能与SO2反应的:X、Y、Z、W |
分析 W是组成信息高速公路骨架的元素之一,应为Si元素,根据X、Y、Z、W在元素周期表中的位置可知X为C元素,Y为N元素,Z为Al元素,结合对应单质、化合物的性质以及元素周期率知识解答该题.
解答 解:W是组成信息高速公路骨架的元素之一,应为Si元素,根据X、Y、Z、W在元素周期表中的位置可知X为C元素,Y为N元素,Z为Al元素,
A.Z为Al,最高化合价为+3价,而Y为N,最高化合价为+5价,故A错误;
B.同周期元素从左到右原子半径逐渐减小,则X>Y、Z>W,故B错误;
C.非金属性N>C>Si>Al,元素的非金属性越强,对应的最高价氧化物对应水化物的酸性越强,故C错误;
D.最高价含氧酸的钠盐分别为Na2CO3、NaNO3、NaAlO2、Na2SiO3,由于亚硫酸酸性比碳酸、硅酸强,则二氧化硫可与Na2CO3、Na2SiO3溶液反应生成二氧化碳、硅酸,NaAlO2溶液与二氧化硫反应生成氢氧化铝沉淀,二氧化硫水溶液呈酸性,而硝酸根离子在酸性条件下具有强氧化性,则NaNO3可与二氧化硫在溶液中发生氧化还原反应,故D正确.
故选D.
点评 本题考查位置、结构、性质的关系及应用,把握元素在周期表中的位置及元素周期律为解答的关键,注意利用实例分析,侧重分析能力和归纳能力的考查,题目难度不大.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
9.如表实验方案设计中,不能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 验证乙烯与溴发生加成反应 | 乙烯通入溴水中,测定反应前后溶液pH |
| B | 检验氯化铁溶液中是否含FeCl2 | 向氯化铁溶液中滴加铁氰化钾溶液 |
| C | 检验乙酸中是否混有乙醇 | 取样液于试管,加入一绿豆颗粒大的钠粒 |
| D | 验证Ksp(AgI)<Ksp(AgCl) | 向含等物质的量NaCl、KI的混合液中滴加AgNO3溶液 |
| A. | A | B. | B | C. | C | D. | D |
1.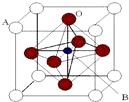 某钙钛型复合氧化物(如图),以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物的电阻率在有外磁场作用时较之无外磁场作用时存在巨大变化(巨磁电阻效应).
某钙钛型复合氧化物(如图),以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物的电阻率在有外磁场作用时较之无外磁场作用时存在巨大变化(巨磁电阻效应).
(1)用A、B、O表示这类特殊晶体的化学式ABO3.在图中,与A原子配位的氧原子数目为12.
(2)基态Cr原子的核外电子排布式为1s22s22p63s23p63d54s1,其中电子的运动状态有24种.
(3)某些钙钛型复合氧化物能够催化NO直接分解为N2和O2,N和O的基态原子中,未成对的电子数目比为3:2.
(4)下表是几种碳酸盐的热分解温度和阳离子半径
请解释碳酸钙热分解温度最低的原因:碳酸盐的热分解是由于晶体中的阳离子结合碳酸根中的氧离子,使碳酸根分解为二氧化碳分子的结果.钙离子由于半径小和氧离子结合更为容易,氧化钙晶格能大,所以碳酸钙分解温度低.
(5)用晶体的X射线衍射法可以测得阿伏伽德罗常数.对金属钙的测定得到以下结果:晶胞为面心立方最密堆积,边长为558pm.又知钙的密度为1.54g•cm-3,则1cm3钙晶体中含有5.76×1021个晶胞,阿伏伽德罗常数为$\frac{40g/mol×4×5.76×1{0}^{21}}{1.54g/c{m}^{3}×1c{m}^{3}}$=6.0×1023(列式计算).
 某钙钛型复合氧化物(如图),以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物的电阻率在有外磁场作用时较之无外磁场作用时存在巨大变化(巨磁电阻效应).
某钙钛型复合氧化物(如图),以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物的电阻率在有外磁场作用时较之无外磁场作用时存在巨大变化(巨磁电阻效应).(1)用A、B、O表示这类特殊晶体的化学式ABO3.在图中,与A原子配位的氧原子数目为12.
(2)基态Cr原子的核外电子排布式为1s22s22p63s23p63d54s1,其中电子的运动状态有24种.
(3)某些钙钛型复合氧化物能够催化NO直接分解为N2和O2,N和O的基态原子中,未成对的电子数目比为3:2.
(4)下表是几种碳酸盐的热分解温度和阳离子半径
| 碳酸盐 | CaCO3 | SrCO3 | BaCO3 |
| 热分解温度/℃ | 900 | 1172 | 1360 |
| 阳离子半径/pm | 99 | 112 | 135 |
(5)用晶体的X射线衍射法可以测得阿伏伽德罗常数.对金属钙的测定得到以下结果:晶胞为面心立方最密堆积,边长为558pm.又知钙的密度为1.54g•cm-3,则1cm3钙晶体中含有5.76×1021个晶胞,阿伏伽德罗常数为$\frac{40g/mol×4×5.76×1{0}^{21}}{1.54g/c{m}^{3}×1c{m}^{3}}$=6.0×1023(列式计算).
7.化学与生活密切相关,下列有关说法正确的是( )
| A. | Li是最轻的金属,也是活动性极强的金属,是制造电池的理想物质 | |
| B. | 工厂中常用的静电除尘装置是根据胶体带电这个性质而设计的 | |
| C. | 由于铝的导电性比铜、银都强,所以常用来制造电线、电缆 | |
| D. | NH3能氧化氮氧化物,可用于汽车尾气净化 |
4.下列各组物质中互为同位素的是( )
| A. | 氕和氘 | B. | H2O和D2O | C. | 石墨和金刚石 | D. | CH4和C3H8 |
5.在无色透明的酸性溶液中,能大量共存的离子组是( )
| A. | Al3+、NH4+、Cl-、HCO3- | B. | Na+、NO3-、SO42-、I- | ||
| C. | Na+、Mg2+、Cl-、SO42- | D. | Fe3+、K+、Cl-、NO3- |
 ↑
↑ +OH-+ Ba2+ = BaSO4↓+H2O
+OH-+ Ba2+ = BaSO4↓+H2O