题目内容
9.下列有关元素周期律的叙述中正确的是( )| A. | 氧化性:F2<Cl2 | B. | 气态氢化物的稳定性:H2O<H2S | ||
| C. | 酸性:H3PO4<H2SO4 | D. | 粒子半径:Na+>Na |
分析 A.元素的非金属性越强,其单质的氧化性越强;
B.元素的非金属性越强,其气态氢化物的稳定性越强;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强;
D.原子或离子电子层数越多其半径越大.
解答 解:A.元素的非金属性越强,其单质的氧化性越强,非金属性F>Cl,所以氧化性F2>Cl2,故A错误;
B.元素的非金属性越强,其气态氢化物的稳定性越强,非金属性O>S,则气态氢化物的稳定性:H2O>H2S,故B错误;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强,非金属性S>P,所以酸性:H3PO4<H2SO4,故C正确;
D.原子或离子电子层数越多其半径越大,Na有3个电子层、钠离子有2个电子层,所以半径:Na+<Na,故D错误;
故选C.
点评 本题考查元素周期律,侧重考查非金属性强弱判断,明确非金属性强弱与单质的氧化性、氢化物的稳定性、最高价含氧酸的酸性之间关系是解本题关键,知道非金属性强弱判断方法,题目难度不大.

练习册系列答案
相关题目
19.NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA个 | |
| B. | 11.2 L NH3中所含的原子数为2NA | |
| C. | 2.4g金属镁变为Mg2+时失去的电子数为0.1 NA | |
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA个 |
14.最近湖南都市台报道,长沙市周边农田由于焚烧稻草导致烟雾弥漫,致使高速公路限行,航班停飞.烟雾属于下列分散系中的( )
| A. | 溶液 | B. | 悬浊液 | C. | 乳浊液 | D. | 胶体 |
1.下列离子能大量共存的是( )
| A. | 使酚酞试液变红的溶液:Na+,K+,SO${\;}_{4}^{2-}$,HCO${\;}_{3}^{-}$ | |
| B. | 无色透明的溶液中:MnO${\;}_{4}^{-}$,K+,SO${\;}_{4}^{2-}$,Na+ | |
| C. | 含有大量Mg2+的溶液中:Fe2+,SO${\;}_{4}^{2-}$,NO${\;}_{3}^{-}$,Cl- | |
| D. | 使紫色石蕊试液变红的溶液:NH${\;}_{4}^{+}$,NO${\;}_{3}^{-}$,Al3+,CH3COO- |
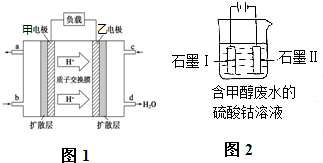 甲醇是一种重要燃料,在电化学领域有着重要的用途.
甲醇是一种重要燃料,在电化学领域有着重要的用途.