题目内容
【题目】已知X、Y、Z、R、Q为周期表中原子序数依次增大的前36号元素。相关信息如下:
X元素是宇宙中最丰富的元素 |
Y元素基态原子的核外p电子数比s电子数少1 |
Z元素被誉为“太空金属”,也有“生物金属”之称,其基态原子次外层有2个未成对电子 |
R元素在元素周期表的第十一列 |
Q元素在周期表里与R元素在同一个分区 |
请回答下列问题:
(1)YX3中心原子的杂化轨道类型是________________,离子化合物YX5的电子式是_________。
(2)CO与Y2属于等电子体,1 个CO分子中含有的π键数目是________个。
(3)工业上利用ZO2和碳酸钡在熔融状态下制取化合物A(A可看做一种含氧酸盐)。A晶体的晶胞为正方体(如图)。
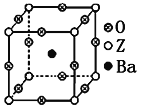
①制备A的化学方程式是_________________________________________;
②在A晶体中,Z的配位数为_______________;
③在A晶体中,若将Z元素置于立方体的体心,Ba元素置于立方体的顶点,则O元素处于立方体的______________。
(4)R2+离子的外围电子层电子排布式为______________。R2O的熔点比R2S的________(填“高”或“低”)。
(5)Q元素和硫(S)元素能够形成化合物B。B晶体的晶胞为正方体(如图),若晶胞棱长为540.0 pm,则晶胞密度为___________________________g·cm3(列式并计算)。
 。
。
【答案】sp3杂化 ![]() 2 TiO2+BaCO3
2 TiO2+BaCO3![]() BaTiO3+CO2↑ 6 面心 3d9 高
BaTiO3+CO2↑ 6 面心 3d9 高 ![]() =4.1
=4.1![]()
【解析】
根据题给信息推断X为氢元素,Y为氮元素,Z为钛元素,R为铜元素,Q为锌元素。
(1)NH3分子中含有3个键,氮原子有1对孤对电子,中心原子的杂化轨道类型是sp3,离子化合物NH5的电子式是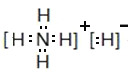 ;
;
(2)N2的结构式为N≡N,两个成键原子间有且只有1个键,CO与N2属于等电子体,故1 个CO分子中含有的π键数目是2个;
(3)①根据A的晶胞结构利用切割法计算,1个晶胞中含钡数目为1,含钛数目为8×1/8=1,含氧数目为12×![]() =3,A的化学式为BaTiO3。TiO2和碳酸钡在熔融状态下反应生成BaTiO3和二氧化碳,化学方程式为TiO2+BaCO3= BaTiO3+CO2↑;②在A晶体中,Ti的配位数为6(上、下、前、后、左、右均与O直接相连);③在A晶体中,若将Z元素置于立方体的体心,Ba元素置于立方体的顶点,则O元素处于立方体的面心;
=3,A的化学式为BaTiO3。TiO2和碳酸钡在熔融状态下反应生成BaTiO3和二氧化碳,化学方程式为TiO2+BaCO3= BaTiO3+CO2↑;②在A晶体中,Ti的配位数为6(上、下、前、后、左、右均与O直接相连);③在A晶体中,若将Z元素置于立方体的体心,Ba元素置于立方体的顶点,则O元素处于立方体的面心;
(4)R为铜元素,原子序数为29,根据构造原理判断Cu2+离子的外围电子层电子排布式为3d9。Cu2O和Cu2S为结构相似的离子晶体,离子所带的电荷相同,氧离子半径小于硫离子半径,氧化亚铜的晶格能大于硫化亚铜的晶格能,故Cu2O的熔点比Cu2S的高;
(5)ZnS晶胞中含硫原子数目为8×1/8+6×1/2=4,含锌原子数目为4,则1mol晶胞的质量为4×(65+32)g,晶胞为正方体,若晶胞棱长为540.0 pm,则晶胞密度为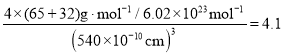 g·cm—3。
g·cm—3。

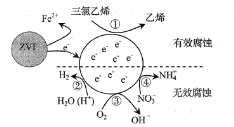
【题目】科学家研究出一种以天然气为燃料的“燃烧前捕获系统”,其简单流程如图所示(条件及物质未标出)。
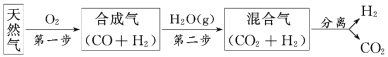
(1)已知:CH4、CO、H2的燃烧热分别为890.3 kJ·mol-1、283.0 kJ·mol-1、285.8 kJ·mol-1,则上述流程中第一步反应2CH4(g)+O2(g)===2CO(g)+4H2(g)的ΔH=______________。
(2)工业上可用H2和CO2制备甲醇,其反应方程式为CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),某温度下,将1 mol CO2和3 mol H2充入体积不变的2 L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表:
CH3OH(g)+H2O(g),某温度下,将1 mol CO2和3 mol H2充入体积不变的2 L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表:
时间/h | 1 | 2 | 3 | 4 | 5 | 6 |
| 0.90 | 0.85 | 0.83 | 0.81 | 0.80 | 0.80 |
①用H2表示前2 h 的平均反应速率v(H2)=_________________________________;
②该温度下,CO2的平衡转化率为________。
(3)在300 ℃、8 MPa下,将CO2和H2按物质的量之比1∶3 通入一密闭容器中发生(2)中反应,达到平衡时,测得CO2的平衡转化率为50%,则该反应条件下的平衡常数为Kp=________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)CO2经催化加氢可合成低碳烯烃:2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g) ΔH。在0.1 MPa时,按n(CO2)∶n(H2)=1∶3投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
C2H4(g)+4H2O(g) ΔH。在0.1 MPa时,按n(CO2)∶n(H2)=1∶3投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
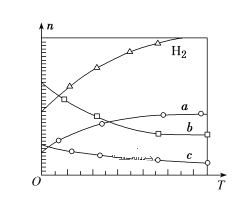
①该反应的ΔH________0(填“>”或“<”)。
②曲线c表示的物质为_______。
③为提高H2的平衡转化率,除改变温度外,还可采取的措施______________。(答出一条即可)