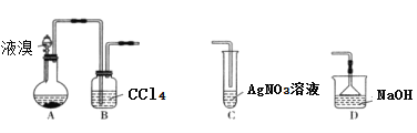
题目内容
【题目】已知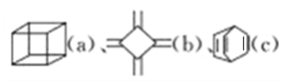 的分子式均为C8H8,下列说法正确的是( )
的分子式均为C8H8,下列说法正确的是( )
A.c可与酸性高锰酸钾溶液反应,a和b不行
B.a、b 的二氯代物均有3种,c的二氯代物有6种
C.a的同分异构体中除b、c外,还可以是苯的同系物
D.a、b、c中只有b、c的所有原子处于同一平面
【答案】B
【解析】
A.b和c分子结构中均含有碳碳双键,能使酸性高锰酸钾溶液褪色,而a不含碳碳双键,与酸性高锰酸钾不反应,故A错误;
B.a中只有一个等效氢,一氯代物只有一种,为立方体的顶点,当顶点有一氯原子时,等效氢是3种,则二氯代物共有3种;b中只有一个等效氢,一氯代物只有一种,为CH2=上的一个氢原子被取代,当CH2=上有一氯原子时,剩余等效氢是3种,则二氯代物共有3种;c中,如一个Cl位于1个饱和碳原子,则另一个Cl原子有3种位置,两个Cl原子也可都在C=C键,或不同的C=C键位置,即二氯代物共有6种,故B正确;
C.a的同分异构体中除b、c外,还可以是苯乙烯,但不是苯的同系物,故C错误;
D.c含有饱和碳原子,具有甲烷的结构特点,而b中与碳碳双键直接相连的原子在同一个平面上,则b的所有原子处于同一平面,c中所有原子不可能在同一平面内,故D错误;
故答案为B。

【题目】利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中Cr(III)的处理工艺流程如下。
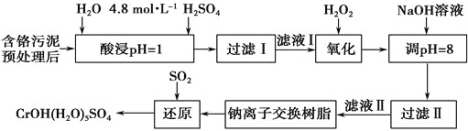
其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
(1)酸浸时,为了提高浸取率可采取的措施有______________![]() 答出两点
答出两点![]() 。
。
(2)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:_____________。
(3)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
开始沉淀时的pH | 2.7 |
|
|
|
沉淀完全时的pH | 3.7 | 11.1 | 8 | 9(>9溶解) |
加入NaOH溶液使溶液呈碱性,Cr2O72-转化为CrO42-。滤液Ⅱ中阳离子主要有________;但溶液的pH不能超过8,其理由是_______________。
(4)写出上述流程中用SO2进行还原时发生反应的化学方程式: ____________。
(5)滴定法测定纯碱产品中NaHCO3含量的方法是:准确称取纯碱样品Wg,放入锥形瓶中加蒸馏水溶解,加1~2滴酚酞指示剂,用cmol/L的HCl溶液滴定至溶液由红色变为无色![]() 指示
指示![]() 反应的终点
反应的终点![]() ,所用HCl溶液体积为V1mL,再加1~2滴甲基橙指示剂,继续用HCl溶液滴定至溶液由黄色变为橙色,所用HCI溶液总体积为V2mL,则纯碱样品中NaHCO3质量分数为____________。
,所用HCl溶液体积为V1mL,再加1~2滴甲基橙指示剂,继续用HCl溶液滴定至溶液由黄色变为橙色,所用HCI溶液总体积为V2mL,则纯碱样品中NaHCO3质量分数为____________。
【题目】己知HNO2在低温下较稳定,既有氧化性又有还原性,其氧化产物、还原产物与溶液pH的关系如下表,且酸性:![]() 。下列有关说法错误的是
。下列有关说法错误的是![]()
![]()
pH范围 |
|
|
产物 |
| NO、 |
A.碱性条件下,NaNO2与NaClO反应的离子方程式为![]()
B.向冷的NaNO2溶液中通入H2S气体,有淡黄色沉淀产生
C.低温时不用其它试剂即可区分HNO2溶液与Na2CO3溶液
D.向冷的NaNO2溶液中通入SO2可得到HNO2
【题目】类比推理是学习化学的重要的思维方法,下列陈述Ⅰ及类比推理陈述Ⅱ均正确的是( )
陈述Ⅰ | 类比推理陈述Ⅱ | |
A | 单质的熔点Br2 < I2 | 单质的熔点Li < Na |
B | 工业上电解熔融的Al2O3得到铝单质 | 工业上电解熔融的MgO得到镁单质 |
C | 还原性:I- > Br- | 还原性:P3- > N3- |
D | 溶解度:CaCO3<Ca(HCO3)2 | 溶解度:Na2CO3<NaHCO3 |
A.AB.BC.CD.D