题目内容
【题目】已知25 ℃时Ksp[Mg(OH)2]=5.6×10-12,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Al(OH)3]=1.1×10-33
(1)①在25 ℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成________沉淀(填化学式)。
②用MgCl2、AlCl3的混合溶液(A)与过量氨水(B)反应,为使Mg2+、Al3+同时生成沉淀,应先向沉淀反应器中加入________(填“A”或“B”),再滴加另一反应物。
(2)①Fe3+发生水解反应Fe3++3H2O![]() Fe(OH)3+3H+,该反应的平衡常数为________。
Fe(OH)3+3H+,该反应的平衡常数为________。
②若向FeCl3溶液中加入一定量石灰水,调节溶液pH,可得红褐色沉淀。该过程中调节溶液的pH为5,则金属离子浓度为________。
(3)溶液中某离子物质的量浓度低于1.0×10-5 mol·L-1时,可认为已沉淀完全。现向一定浓度的AlCl3和FeCl3的混合溶液中逐滴加入氨水,当Fe3+完全沉淀时,测定c(Al3+)=0.2 mol·L-1。此时所得沉淀中________(填“还含有”或“不含有”)Al(OH)3。
【答案】 Cu(OH)2 B  4×10-11mol/L 不含有
4×10-11mol/L 不含有
【解析】(1)①溶度积常数越小的物质越先沉淀,氢氧化铜的溶度积小于氢氧化镁的溶度积,所以氢氧化铜先沉淀;②同时生成沉淀,应先将氨水加入沉淀反应器中,答案选B;(2)①根据方程式可知该反应的平衡常数为 ;②溶液的pH为5,即氢氧根浓度是10-9mol/L,则金属离子浓度为
;②溶液的pH为5,即氢氧根浓度是10-9mol/L,则金属离子浓度为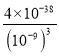 =4×10-11mol/L ;(3)当Fe3+完全沉淀时溶液中c3(OH-)=Ksp/c(Fe3+)=4×10-33,此时溶液中有:c(Al3+)×c3(OH-)=0.2×4×10-33=8×10-34<1.1×10-33,无氢氧化铝沉淀生成,故不含有。
=4×10-11mol/L ;(3)当Fe3+完全沉淀时溶液中c3(OH-)=Ksp/c(Fe3+)=4×10-33,此时溶液中有:c(Al3+)×c3(OH-)=0.2×4×10-33=8×10-34<1.1×10-33,无氢氧化铝沉淀生成,故不含有。

 阅读快车系列答案
阅读快车系列答案【题目】实验题
(一)实验室中有一瓶含有一定量杂质的烧碱样品,某学生用中和滴定法测定烧碱的纯度,若烧碱中所含杂质与酸不反应,请根据实验回答:

(1)将准确称取的5g烧碱样品配成100 mL待测液,需要的主要仪器除量筒、烧杯、玻璃棒、托盘天平外,还必须用到的仪器有:____________、_____________。
(2)取10.00 mL待测液,选择右图中_________(填A或B)来移取。
(3)用0.5000mol/L标准盐酸滴定待测烧碱溶液,以酚酞为指示剂。滴定时左手旋转滴定管玻璃活塞,右手不停地摇动锥形瓶,两眼注视___________________,直到滴定终点。滴定达到终点的标志是:_______________________________。
(4)根据下列数据,烧碱的纯度为:_______________________
滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 10.00 | 0.50 | 20.40 |
第二次 | 10.00 | 4.00 | 24.10 |
(5)判断下列操作引起的误差(填偏大、偏小或无影响)
①滴定前读数正确,滴定终点读数时仰视_________________
②装待测液前,锥形瓶内残留少量蒸馏水_______________
(二)氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。测血钙的含量时,进行如下实验:
①可将2mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成 CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去20mL l.0×l0﹣4 mol/L的KMnO4溶液。
(1)写出用KMn04滴定H2C2O4的离子方程式_____________________。
(2)滴定时,将KMnO4溶液装在________(填“酸式”或“碱式”)滴定管中。
(3)误差分析:(填“偏高”、“偏低”或“无影响”)
①如果滴定管用蒸馏水洗后未用酸性KMnO4标准液润洗,则测量结果________。
②滴定前后读数都正确,但滴定前有气泡,而滴定后气泡消失,则测量结果________。
(4)计算:血液中含钙离子的浓度为_____mol·L-1。
