题目内容
【题目】已知:(HF)2(g) ![]() 2HF(g) △H>0,平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
2HF(g) △H>0,平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
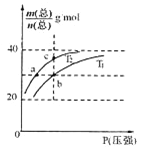
A.温度:T1< T2
B.平衡常数:K(a)=K(b)<K(c)
C.反应速率:v(b)>v(a)
D.当![]() 30g·mol-1时,n(HF):n[(HF)2]=2:1
30g·mol-1时,n(HF):n[(HF)2]=2:1
【答案】C
【解析】
试题分析:A.反应:(HF)2(g) ![]() 2HF(g) △H>0的正反应是吸热反应,在压强不变时,升高温度,平衡正向移动,气体的物质的量增大,平衡体系的总质量m(总)与总物质的量n(总)之比减小。因此温度: T1 > T2。A 错误。B.化学平衡常数只与温度有关,而与压强无关。由于a、c在温度T2线上,b在温度T1线上。升高温度化学平衡正向移动,化学平衡常数增大,所以K(a)= K(c) < K(b)。B错误。C.由于b点的温度比a点高,压强比a点大,升高温度,化学反应速率加快;增大压强,化学反应速率加快,故化学反应速率v(b)>v(a),C正确。D.若n(HF):n[(HF)2]=2:1,则
2HF(g) △H>0的正反应是吸热反应,在压强不变时,升高温度,平衡正向移动,气体的物质的量增大,平衡体系的总质量m(总)与总物质的量n(总)之比减小。因此温度: T1 > T2。A 错误。B.化学平衡常数只与温度有关,而与压强无关。由于a、c在温度T2线上,b在温度T1线上。升高温度化学平衡正向移动,化学平衡常数增大,所以K(a)= K(c) < K(b)。B错误。C.由于b点的温度比a点高,压强比a点大,升高温度,化学反应速率加快;增大压强,化学反应速率加快,故化学反应速率v(b)>v(a),C正确。D.若n(HF):n[(HF)2]=2:1,则![]()
![]() =26.7g/mol<30g/mol。D错误。故选C。
=26.7g/mol<30g/mol。D错误。故选C。

练习册系列答案
相关题目


