题目内容
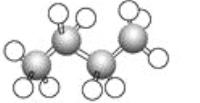
【题目】下图为正丁烷的球棍模型。下列说法正确的是( )
A. 正丁烷的分子式为C4H8
B. 分子中4个碳原子在同一条直线上
C. 分子中含有4个C—C单键
D. 分子中共含有13个共价键
【答案】D
【解析】分析:由正丁烷的球棍模型可以写出其分子式为C4H10,分子中4个碳原子形成的碳链为锯齿状;分子中的4个碳原子形成3个C—C单键,10个氢原子形成10个C—H单键,共形成13个共价键。
由正丁烷的球棍模型可以写出其分子式为C4H10,属于烷烃,A错误;甲烷分子为正四面体构型,因此该分子中4个碳原子形成的碳链为锯齿状,不可能4个碳原子在同一条直线上,B错误;根据正丁烷的球棍模型可以知道,分子中含有3个C—C单键,C错误;氢原子与碳原子间形成10条共价键,碳碳原子间形成3条共价键,共计含有13个共价键,D正确;正确选项D。
点睛;甲烷是最简单的烷烃,由于甲烷为正四面体结构,因此烷烃的结构中,相当于含有-CH3、 -CH2- 、 ![]() 、
、![]() 结构,所以烷烃均为空间构型,不是平面构型。
结构,所以烷烃均为空间构型,不是平面构型。

练习册系列答案
相关题目