题目内容
已知:家用消毒液的主要成分是NaClO和NaCl,通常由氯气与氢氧化钠反应来制取.请判断下列反应需加入适当氧化剂才能实现的是( )
| A、Cl2→NaClO |
| B、MnO2→Mn2+ |
| C、SO2→SO32- |
| D、PCl3→PCl5 |
考点:重要的氧化剂
专题:氧化还原反应专题
分析:A.Cl2→NaClO:氯气与氢氧化钠反应可实现,无需加入氧化剂;
B.MnO2→Mn2+:Mn的化合价由+4价降低到+2价,化合价降低,被还原,需加入适当还原剂才能实现;
C.SO2→SO32-:元素的化合价没有发生变化,故无需加入氧化剂;
D.PCl3→PCl5:P的化合价由+3价升高到+5价,化合价升高,被氧化,故需加入适当氧化剂才能实现.
B.MnO2→Mn2+:Mn的化合价由+4价降低到+2价,化合价降低,被还原,需加入适当还原剂才能实现;
C.SO2→SO32-:元素的化合价没有发生变化,故无需加入氧化剂;
D.PCl3→PCl5:P的化合价由+3价升高到+5价,化合价升高,被氧化,故需加入适当氧化剂才能实现.
解答:
解:A.Cl2→NaClO:氯气与氢氧化钠反应可实现,无需加入氧化剂,故A错误;
B.MnO2→Mn2+:Mn的化合价由+4价降低到+2价,化合价降低,被还原,需加入适当还原剂才能实现,故B错误;
C.SO2→SO32-:元素的化合价没有发生变化,故无需加入氧化剂,故C错误;
D.PCl3→PCl5:P的化合价由+3价升高到+5价,化合价升高,被氧化,故需加入适当氧化剂才能实现,故D正确,
故选D.
B.MnO2→Mn2+:Mn的化合价由+4价降低到+2价,化合价降低,被还原,需加入适当还原剂才能实现,故B错误;
C.SO2→SO32-:元素的化合价没有发生变化,故无需加入氧化剂,故C错误;
D.PCl3→PCl5:P的化合价由+3价升高到+5价,化合价升高,被氧化,故需加入适当氧化剂才能实现,故D正确,
故选D.
点评:本题考查氧化还原反应,难度不大.要注意还原剂在化学反应中失去电子,化合价升高.

练习册系列答案
相关题目
现有V L 0.5mol/L的盐酸,欲将其浓度扩大一倍,以下方法中最宜采用的是( )
| A、加热浓缩到原来体积的一半 |
| B、加入0.05mol/L的盐酸0.125V L |
| C、加入10mol/L的盐酸0.1V L,再稀释至1.5 V L |
| D、标况下通入11.2L氯化氢气体 |
某二种气态混合烃1L,完全燃烧后生成1.4L CO2和1.6L水蒸气(体积均在相同条件下测得),该混合烃是( )
| A、乙烷、乙炔 |
| B、甲烷、乙炔 |
| C、甲烷、丙炔 |
| D、乙烷、丙炔 |
水溶液中能大量共存的一组离子是( )
| A、Na+、Al3+、Cl-、HCO3- |
| B、H+、Fe2+、NO3-、SO42- |
| C、H+、Mg2+、Cl-、NO3- |
| D、K+、Ag+、OH-、SO42- |
X、Y、Z、W、Q均为含氮的化合物,在一定条件下,将发生如下转换关系(未配平):
①X→W+O2
②Z+Y+NaOH→H2O+W
③Y+SO2→Z+SO3
④Q+Y→Z+H2O
⑤X+Cu+H2SO4→Cu2++Y+SO42-
这五种化合物中氮元素的化合价由高到低的顺序为( )
①X→W+O2
②Z+Y+NaOH→H2O+W
③Y+SO2→Z+SO3
④Q+Y→Z+H2O
⑤X+Cu+H2SO4→Cu2++Y+SO42-
这五种化合物中氮元素的化合价由高到低的顺序为( )
| A、XYZWQ |
| B、XZYQW |
| C、XYWZQ |
| D、WXZQY |
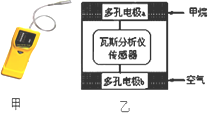 有一种瓦斯分析仪(如图甲),工作原理类似燃料电池,其装置如图乙所示,其中的固体电解质是Y2O3-Na2O,O2-可以在其中自由移动.下列有关叙述正确的是( )
有一种瓦斯分析仪(如图甲),工作原理类似燃料电池,其装置如图乙所示,其中的固体电解质是Y2O3-Na2O,O2-可以在其中自由移动.下列有关叙述正确的是( )| A、瓦斯分析仪工作时,电池内电路中电子由电极b流向电极a |
| B、电极b是正极,O2-由电极a流向电极b |
| C、电极a的反应式为:CH4+5O2--8e-═CO32-+2H2O |
| D、当固体电解质中有1mol O2-通过时,电子转移4mol |
在Na与H2O的反应中( )
| A、Na是氧化剂 |
| B、反应实质是钠置换水中的氢气 |
| C、反应实质是钠置换水电离出的少量的H+ |
| D、H2是氧化产物 |
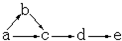 a、b、c、d、e是含有一种相同元素的五种物质,可发生如下转化:
a、b、c、d、e是含有一种相同元素的五种物质,可发生如下转化: