题目内容
5. 冰晶石(化学式为Na3AlF6)的晶体结构单元如图所示(位于大立方体的定点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心),已知冰晶石熔融时电离方程式为:Na3AlF6=3Na++AlF${\;}_{6}^{2-}$,那么大立方体的体心处
冰晶石(化学式为Na3AlF6)的晶体结构单元如图所示(位于大立方体的定点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心),已知冰晶石熔融时电离方程式为:Na3AlF6=3Na++AlF${\;}_{6}^{2-}$,那么大立方体的体心处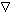 所代表的微粒为( )
所代表的微粒为( )| A. | Na+ | B. | Al3+ | C. | F- | D. | AlF${\;}_{6}^{2-}$ |
分析 该晶胞中●个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,○个数=12×$\frac{1}{4}$+8=11,根据化学式知,冰晶石中阳离子和阴离子个数之比为3:1,据此判断大立方体的体心处▽所代表的微粒.
解答 解:该晶胞中●个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,○个数=12×$\frac{1}{4}$+8=11,根据化学式知,冰晶石中阳离子和阴离子个数之比为3:1,要使阳离子、阴离子个数之比为3:1,则大立方体的体心处▽所代表的微粒是Na+,
故选A.
点评 本题考查了晶胞的计算,题目难度不大,注意把握均摊法在计算中的应用,侧重于考查学生的空间想象能力和计算能力.

练习册系列答案
相关题目
15.某强酸性溶液X中仅含有NH4+、Al3+、Ba2+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种,取该溶液进行连续实验,实验过程如下

下列有关推断合理的是( )

下列有关推断合理的是( )
| A. | 若溶液X为100 mL,产生的气体A为112 mL(标况),则X中c(Fe2+)=0.05 mol•L-1 | |
| B. | 沉淀H为Al(OH)3、BaCO3的混合物 | |
| C. | 溶液中一定含有H+、Al3+、NH4+、Fe2+、SO42-、Cl- | |
| D. | 根据上述连续实验不能确定溶液X中是否含有Fe3+ |
16.碘是人体必需的微量元素,127I的中子数为74,则其原子序数为( )
| A. | 74 | B. | 53 | C. | 201 | D. | 127 |
13.对下列事故预防或处理方法正确的是( )
| A. | 稀释浓硫酸时,为防止液体飞溅,将浓硫酸沿烧杯壁缓缓加入水中,并不断搅拌 | |
| B. | 欲配置500 mL l mol/LNaOH溶液,应将20gNaOH固体溶于500 mL水中 | |
| C. | 浓NaOH溶液溅到皮肤上,立即用水冲洗,然后涂上稀硫酸 | |
| D. | 钠着火时用二氧化碳灭火 |
15. 如图是某学生设计的一个原电池,若要装置中电流计发生偏转,则M、N两极的组成材料及液体X分别是( )
如图是某学生设计的一个原电池,若要装置中电流计发生偏转,则M、N两极的组成材料及液体X分别是( )
 如图是某学生设计的一个原电池,若要装置中电流计发生偏转,则M、N两极的组成材料及液体X分别是( )
如图是某学生设计的一个原电池,若要装置中电流计发生偏转,则M、N两极的组成材料及液体X分别是( )| A. | Cu、石墨、NaOH溶液 | B. | 石墨、石墨、水 | ||
| C. | Cu、Fe、酒精 | D. | Zn、Cu、稀H2SO4溶液 |



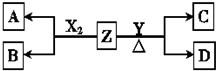 短周期元素组成的单质X2,Y.常温下,X2是一种黄绿色气体,Y为淡黄色固体,Z是一种常见的碱,焰色反应呈浅紫色(透过钴玻璃)且0.1mol•L-1 Z的水溶液pH=13.X2、Y 和Z之间有如图转化关系(其他无关物质已略去)
短周期元素组成的单质X2,Y.常温下,X2是一种黄绿色气体,Y为淡黄色固体,Z是一种常见的碱,焰色反应呈浅紫色(透过钴玻璃)且0.1mol•L-1 Z的水溶液pH=13.X2、Y 和Z之间有如图转化关系(其他无关物质已略去) )为主要成分的天然高分子化合物.天然橡胶有两种,一种是巴西三叶橡胶树产出的橡胶,通常就称为天然橡胶;另一种是杜仲树产出的橡胶,它是我国特产,在湖北等地都有大面积种植,被称为杜仲胶.
)为主要成分的天然高分子化合物.天然橡胶有两种,一种是巴西三叶橡胶树产出的橡胶,通常就称为天然橡胶;另一种是杜仲树产出的橡胶,它是我国特产,在湖北等地都有大面积种植,被称为杜仲胶.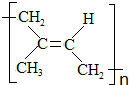 .
.

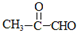 ;
; ;反应类型:酯化反应.
;反应类型:酯化反应.