题目内容
14.以下说法正确的是( )| A. | 同分异构体之间分子式相同,其式量也一定相等,式量相等的物质一定是同分异构体 | |
| B. | 同分异构体之间某种元素的质量分数均相同,化合物之间某种元素质量分数均相同的物质一定为同分异构体 | |
| C. | 两种物质如果互为同分异构体,则一定不可能为同系物 | |
| D. | 两种物质如果互为同分异构体,则它们的命名可能一样 |
分析 A.相对分子质量相同的两种物质分子式不一定相同;
B.各元素质量分数均相同,则最简式相同,分子式不一定相同;
C.同系物分子组成相差一个或若干个CH2原子团;
D.同分异构体的命名是不一样得.
解答 解:A.相对分子质量相同的两种物质分子式不一定相同,如甲酸与乙醇,二者不一定为同分异构体,故A错误;
B.各元素质量分数均相同,则最简式相同,分子式不一定相同,如苯与乙炔,二者不一定为同分异构体,故B错误;
C.同系物分子组成相差一个或若干个CH2原子团,所以两种同系物不可能是同分异构体,故C正确;
D.两种物质如果互为同分异构体,则它们的命名不一样,故D错误,
故选C.
点评 本题考查了同分异构体、同系物,侧重于概念的考查,题目难度不大.

练习册系列答案
相关题目
4.下列说法正确的是( )
| A. | 过氧化钠是既有氧化性又有还原性的淡黄色固体 | |
| B. | 铝箔在酒精灯上灼烧可观察到内部熔化但不滴落,说明铝的熔点高 | |
| C. | SiO2属于酸性氧化物,能和水化合生成硅酸 | |
| D. | 二氧化硅可以用来作太阳能电池的材料 |
5.有关钴和铁化合物的性质见下表
用含钴废料(含少量铁)可制备氯化钴:Co+2HCl═CoCl2+H2↑.工艺流程如下:
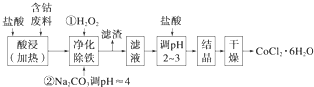
试回答:
(1)“净化除铁”中,写出加入H2O2时反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(2)②步中用Na2CO3调pH≈4的原因是碳酸钠可与盐酸反应,降低溶液的酸性,增大pH,使铁离子沉淀完全.
(3)“滤液”中所含主要溶质的化学式是CoCl2、NaCl、HCl.
(4)为防止CoCl2•6H2O脱水,“干燥”时可采用的方法或操作是减压烘干晶体表面的水分,或常温下晾干,或常温下鼓风吹干,或低于100度小心烘干等.
| 分子式 | 溶度积Ksp | 沉淀完全时的pH | 氯化钴晶体的性质 |
| Co(OH)2 | 5.9×10-15 | 9.4 | CoCl2•6H2O呈红色,常温下稳定.110~120℃时脱水变成蓝色无水氯化钴 |
| Fe(OH)2 | 1.6×10-14 | 9.6 | |
| Fe(OH)3 | 1.1×10-36 | 3.7 |

试回答:
(1)“净化除铁”中,写出加入H2O2时反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(2)②步中用Na2CO3调pH≈4的原因是碳酸钠可与盐酸反应,降低溶液的酸性,增大pH,使铁离子沉淀完全.
(3)“滤液”中所含主要溶质的化学式是CoCl2、NaCl、HCl.
(4)为防止CoCl2•6H2O脱水,“干燥”时可采用的方法或操作是减压烘干晶体表面的水分,或常温下晾干,或常温下鼓风吹干,或低于100度小心烘干等.
2.下列物质属于同分异构体的一组是( )
| A. | 淀粉和纤维素 | B. | CH3CH2CH2CH3 与(CH3)2CHCH3 | ||
| C. | 1H 和2H | D. | O2与O3 |
9.下列有关实验的操作、原理和现象,正确的是( )
| A. | 亚硝酸钠不稳定,常温下即会分解,可用作食品添加剂 | |
| B. | 纸层析实验中,滤纸作为惰性支持物,展开剂作为流动相 | |
| C. | 牙膏中的安息香酸钠、氟化钠等溶于水,水解使溶液显酸性 | |
| D. | 欲分离硝酸钾和氯化钠的混合物(物质的量比为1:1),先将样品溶解,然后加热至表面出现晶膜后冷却,过滤得硝酸钾晶体;将母液加热至大量晶体析出后,用余热蒸干,得氯化钠晶体 |
19.常温下,浓度均为0.1mol/L的4种溶液的pH如表:
下列说法正确的是( )
| 溶质 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 9.7 | 10.3 | 4.0 |
| A. | 0.1mol/L Na2CO3溶液加水,稀释后溶液中所有离子的浓度均减少 | |
| B. | NaHCO3溶液中:c(Na+)+c(H+)=c(HSO3-)+c(OH-)+c(CO32-) | |
| C. | NaHSO3溶液中:c(Na+)>c(HSO${\;}_{3}^{-}$)>c(H2SO3)>c(SCO${\;}_{3}^{2-}$)+c(OH?) | |
| D. | 常温下,相同浓度的H2SO3、H2CO3、HClO三种溶液,pH最小的是H2SO3 |
6. 氨在医药、化肥、国防、轻工业等方面均用途广泛.
氨在医药、化肥、国防、轻工业等方面均用途广泛.
(1)工业合成氨时,合成塔中每生成1mol NH3,放出46kJ的热量.其反应过程的能量变化如图.b值为92,加入催化剂,a值减小(填“增大”“减小”或“不变”,下同).压缩容器体积,b值不变.
(2)已知氢气的燃烧热△H=-285kJ•mol-1,则氨与氧气反应生成氮气和液态水时,每消耗8g氧气反应放出的热量为127.2kJ.
(3)常温下,1mol化学键分解成气态原子所需要的能量用E表示.已知:
c的值为483.8.
 氨在医药、化肥、国防、轻工业等方面均用途广泛.
氨在医药、化肥、国防、轻工业等方面均用途广泛.(1)工业合成氨时,合成塔中每生成1mol NH3,放出46kJ的热量.其反应过程的能量变化如图.b值为92,加入催化剂,a值减小(填“增大”“减小”或“不变”,下同).压缩容器体积,b值不变.
(2)已知氢气的燃烧热△H=-285kJ•mol-1,则氨与氧气反应生成氮气和液态水时,每消耗8g氧气反应放出的热量为127.2kJ.
(3)常温下,1mol化学键分解成气态原子所需要的能量用E表示.已知:
| 共价键 | O=O | N≡N | H-N | H-O |
| E(kJ•mol-1) | 497 | 946 | 390 | c |
3.下列有关乙炔性质的叙述中,既不同于乙烯又不同于乙烷的是( )
| A. | 能完全燃烧生成二氧化碳和水 | |
| B. | 能与溴水发生加成反应 | |
| C. | 能与酸性KMnO4溶液发生氧化还原反应 | |
| D. | 能与HCl反应生成氯乙烯 |
4.已知主族元素A、B、C、D的离子aA(n+1)+、bBn+、cC(n+1)-、dDn-具有相同的电子层结构.则下列叙述正确的是(n为正整数)( )
| A. | 原子序数:a<b<d<c | |
| B. | 离子半径:A(n+1)+>Bn+>C(n+1)->Dn- | |
| C. | 单质的还原性:B>A;单质的氧化性:D>C | |
| D. | 离子的还原性:A(n+1)+>Bn+;离子的氧化性:C(n+1)->Dn- |