题目内容
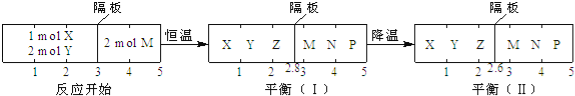
【题目】可逆反应①X(g)+2Y(g)2Z(g)、②2M(g)N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦,可滑动的密封隔板.反应开始和达到平衡状态时有关物理量的变化如图所示:下列判断正确的是( )
A. 反应①的正反应是吸热反应
B. 达平衡(Ⅰ)时体系的压强与反应开始时体系的压强之比为14:15
C. 达平衡(Ⅰ)时,X的转化率为![]()
D. 在平衡(Ⅰ)和平衡(Ⅱ)中,M的体积分数相等
【答案】C
【解析】试题分析:已知反应②反应前后气体的物质的量不变。恒温达平衡(Ⅰ)时, 隔板左右两边体系压强相同, 由阿伏加德罗定律得n(①)/n(②)="V(①)/V(②)," 反应①达平衡(Ⅰ)时气体的物质的量为: n(①)="2×2.8/2.2" mol="28/11" mol, 达平衡(Ⅰ)时体系气体的总物质的量为: 28/11 mol+2 mol="50/11" mol, 由阿伏加德罗定律知平衡(Ⅰ)与反应开始时体系的压强之比为50/11∶5="10∶11," B项错误; 由题意得
X(g) + 2Y(g)![]() 2Z(g)
2Z(g)
反应前 1 mol 2 mol 0
变化量 α mol 2α mol 2α mol
平衡(Ⅰ) (1-α)mol (2-2α)mol 2α mol
1-α+2-2α+2α=28/11,解得α=5/11,C项正确;降温后达平衡(Ⅱ),隔板左边体系体积减小,说明反应①中平衡向正反应方向移动,故正反应为放热反应,A项错误;平衡(Ⅰ)与平衡(Ⅱ)温度不同,平衡状态一定不同,M的体积分数不相等,D项错误。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】

⑴如图所示的仪器中配制溶液肯定不需要的是 (填序号),仪器C的名称是 ,本实验所需玻璃仪器E规格为 mL。
⑵下列操作中,容量瓶所不具备的功能有 (填序号)。
A.配制一定体积准确浓度的标准溶液 | B.长期贮存溶液 |
C.用来加热溶解固体溶质 | D.量取一定体积的液体 |
⑶在配制NaOH溶液实验中,其他操作均正确。若定容时仰视刻度线, 则所配制溶液浓度 0.1 mol/L(填“大于”“等于”或“小于”,下同);若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度 0.1 mol/L。
⑷由计算得知,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸体积为 mL(计算结果保留一位小数)。如果实验室有10 mL、25mL、50 mL量筒,应选用 mL规格的量筒最好。
