题目内容
在相同温度下,体积均为1 L的四个密闭容器中,保持温度和容积不变,以四种不同的投料方式进行反应。平衡时有关数据如下(已知2SO2(g)+O2(g) 2SO3(g)ΔH=-196.6 kJ·mol-1)。
2SO3(g)ΔH=-196.6 kJ·mol-1)。
下列关系正确的是( )
A.a=c;e=g B.a>2b;e>2f C.a>d;e>h D.c+98.3e>196.6
 2SO3(g)ΔH=-196.6 kJ·mol-1)。
2SO3(g)ΔH=-196.6 kJ·mol-1)。| 容器 | 甲 | 乙 | 丙 | 丁 |
| 起始投料量 | 2 mol SO2+1 mol O2 | 1 mol SO2+0.5 mol O2 | 2 mol SO3 | 2 mol SO2+2 mol O2 |
| 反应放出或吸收的热量(kJ) | a | b | c | d |
| 平衡时c(SO3) (mol·L-1) | e | f | g | h |
下列关系正确的是( )
A.a=c;e=g B.a>2b;e>2f C.a>d;e>h D.c+98.3e>196.6
B
试题分析:A、甲与丙的初始用量相当,会建立相同(等效)平衡,只不过建立平衡时反应的方向不同,所以e=g 而且a≠c,错误;B、甲与乙相比较,甲的用量比乙多一倍,在温度和体积相同的条件下,甲中平衡的建立可以在两个乙的基础上,再压缩为1L,但压缩时平衡会右移,所以a>2b,e>2f ,正确;C、甲与丁相比较,丁的平衡可以在甲平衡的基础上再增加1mol氧气,但平衡会向右移动,错误;D、设反应 2SO2 + O2 =" 2SO3" 的转化率为m,则有:e=m所以,反应 2SO3 =" 2SO2" + O2 的转化率为1-m,则:c=+196.6(1-m)所以,c+98.3e=196.6,错误。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
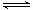 pC(g)+qD(g) △H<0。下列结论中错误的是
pC(g)+qD(g) △H<0。下列结论中错误的是 2HI(g) ΔH =" -14.9" kJ/mol。在甲、乙两个体积相同密闭容器中充入反应物,保持恒温恒容,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)="0.008" mol/L。 下列判断正确的
2HI(g) ΔH =" -14.9" kJ/mol。在甲、乙两个体积相同密闭容器中充入反应物,保持恒温恒容,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)="0.008" mol/L。 下列判断正确的 C(g) △H=" -a" kJ·mol-1,反应达到平衡状态时生成1 mol C气体,放出热量Q1kJ;乙中加入1molC气体,反应达到平衡时,吸收热量Q2kJ,则Q1 与Q2的相互关系正确的是( )
C(g) △H=" -a" kJ·mol-1,反应达到平衡状态时生成1 mol C气体,放出热量Q1kJ;乙中加入1molC气体,反应达到平衡时,吸收热量Q2kJ,则Q1 与Q2的相互关系正确的是( )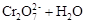

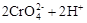 ,下列说法正确的是
,下列说法正确的是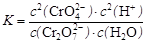
 zC(g),平衡时,测得A的浓度为0.50 mol/L,在温度不变时,把容器容积扩大到原来的2倍,使其重新达到平衡,A的浓度为0.30 mol/L,有关叙述不正确的是( )
zC(g),平衡时,测得A的浓度为0.50 mol/L,在温度不变时,把容器容积扩大到原来的2倍,使其重新达到平衡,A的浓度为0.30 mol/L,有关叙述不正确的是( ) 2NH3已达到平衡,下列有关说法正确的 ( )
2NH3已达到平衡,下列有关说法正确的 ( )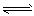 2CrO42-(黄色)+2H+,
2CrO42-(黄色)+2H+, 2 HBr(g) ΔH<0平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是( )
2 HBr(g) ΔH<0平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是( )