��Ŀ����
����Ŀ���±���A��B��C�����л�����й���Ϣ��
A | ����ʹ������Ȼ�̼��Һ��ɫ�������ģ��Ϊ�� |
B | �ٿ��Դ�ú�������ɵ�ú��������ȡ�������ģ��Ϊ�� |
C | �ٹ�ҵ�����п�ͨ��A��H2O�ӳɻ�ã�����Է�������Ϊ46 |
������Ϣ�ش��������⣺
(1)A��������Ȼ�̼��Һ��Ӧ�ķ�Ӧ����Ϊ______��
(2)B��Ũ���ᷢ����Ӧ�Ļ�ѧ����ʽΪ________________��
(3)д��C��ͬ���칹��______________��
(4)��C������ɷ�Ӧ���������仯ѧ����ʽΪ______��
�ڷ�Ӧװ����ͼ��a�Թ������Ƭ��������_______���Թ�b�е��Լ���_______��

���𰸡� �ӳɷ�Ӧ 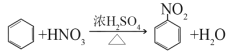 CH3OCH3 CH3COOH+HOCH2CH3
CH3OCH3 CH3COOH+HOCH2CH3![]() CH3COOCH2CH3+H2O ��ֹ���� ���� Na2CO3��Һ
CH3COOCH2CH3+H2O ��ֹ���� ���� Na2CO3��Һ
����������A��ģ�ͼ����ʿ�֪��AΪCH2=CH2��A��ˮ�����ӳɷ�Ӧ����CΪCH3CH2OH��B�к�6��C��6��H��BΪ����Ȼ�����л�������������
��1��A��������Ȼ�̼��Һ��Ӧ�Ļ�ѧ����ʽΪCH2=CH2+Br2��CH2BrCH2Br�����ڼӳɷ�Ӧ���ʴ�Ϊ���ӳɷ�Ӧ��
��2��B��50��60��ʱ��������ᣨŨ�����Ũ����Ļ����Һ����Ӧ���仯ѧ����ʽΪ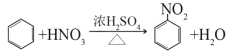 ���ʴ�Ϊ��
���ʴ�Ϊ�� ����3���ʴ�Ϊ��2CH3CH2OH+O2��Cu������Cu2CH3CHO+2H2O��
����3���ʴ�Ϊ��2CH3CH2OH+O2��Cu������Cu2CH3CHO+2H2O��
��4����C��D��Ӧ�Ļ�ѧ����ʽΪCH3COOH+HOCH2CH3![]() CH3COOCH2CH3+H2O���ʴ�Ϊ��CH3COOH+HOCH2CH3
CH3COOCH2CH3+H2O���ʴ�Ϊ��CH3COOH+HOCH2CH3![]() CH3COOCH2CH3+H2O��
CH3COOCH2CH3+H2O��
����������Ҵ��Ļ��Һ�����ʱ������������������a�Թ������Ƭ�������Ƿ�ֹ���У��������������ڱ���̼������Һ�е��ܽ�Ƚ�С��̼�����ܹ��к����ᡢ�ܽ��Ҵ������ڻ��Һ�ֲ㣬����b�е��Լ��DZ��� Na2CO3��Һ��
�ʴ�Ϊ����ֹ���� ������ Na2CO3��Һ��