题目内容
4.下列各组物质按纯净物、电解质、非电解质、能导电的顺序排列的是( )| A. | 烧碱、氯化钠、氯气、氨水 | B. | 纯碱、烧碱、干冰、液态氯化钠 | ||
| C. | 大理石、水、硫酸钡、石墨 | D. | 盐酸、碳酸、氨气、液氨 |
分析 纯净物是指由同种物质组成的;在水溶液里或融融状态下能导电的化合物是电解质;水溶液里或熔融状态下都不能导电的化合物是非电解质;
无论是电解质还是非电解质都必须是化合物,含有自由电子或者自由移动的离子的物质能够导电,据此解答.
解答 解:A.氯气为单质,不是非电解质,故A错误;
B.纯碱是纯净物,烧碱是电解质,干冰是非电解质,液态氯化钠能导电,故B正确;
C.硫酸钡为电解质,故C错误;
D.盐酸是混合物,液氨不导电,故D错误;
故选:B.
点评 本题考查纯净物、混合物、电解质和非电解质的概念,物质导电的条件,明确概念是解题关键,题目难度不大,注意无论是电解质还是非电解质都必须是化合物.

练习册系列答案
相关题目
12.下列实验操作、现象和发生的离子反应完全正确的是( )
| 实验操作 | 现象 | 发生的离子反应 | |
| A | 向BaCl2 溶液中通入CO2 | 溶液浑浊 | Ba2++CO2+H2O═BaCO3↓+2H+ |
| B | 向NaAlO2溶液中滴加过量CO2 | 溶液浑浊 | AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- |
| C | 将可调高度的铜丝伸入到稀HNO3中 | 溶液变蓝 | Cu+4H++2NO3-═Cu2++2NO2↑+2H2O |
| D | 将Cl2通入KI溶液中,加入CCl4,振荡,静置 | 上层溶液显紫红色 | Cl2+2I-═2Cl-+I2 |
| A. | A | B. | B | C. | C | D. | D |
19.下列说法不正确的是( )
| A. | 1 mol氧气的质量为32 g | |
| B. | 常温常压下,1 mol CO2气体体积约为22.4 L | |
| C. | CO2的摩尔质量为44 g•mol-1 | |
| D. | 1 L 2 mol•L-1的BaCl2溶液中含Cl-的个数为2.408×1024 |
9.下列符合实际并用于工业生产的是( )
| A. | 电解氯化钠水溶液来制金属钠 | B. | 氢气和氯气混合后光照制氯化氢 | ||
| C. | 金属钠在氯气中燃烧制氯化钠 | D. | 氯气和石灰乳作用制漂白粉 |
16.对危险化学品要在包装标签上印有警示性标志.下列药品包装图标正确的是( )
| A. |  氢氧化钠 | B. |  红磷 | C. |  硫酸 | D. |  铝合金 |
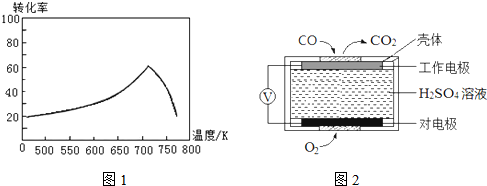
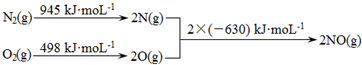
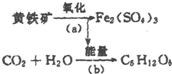 “细菌冶金”是利用某些细菌的特殊代谢功能开采金属矿石.例如溶液中氧化亚铁硫杆菌能利用空气中的氧气将黄铁矿(主要成分为FeS2)氧化为Fe2(SO4)3,并使溶液酸性增强,其过程如图:
“细菌冶金”是利用某些细菌的特殊代谢功能开采金属矿石.例如溶液中氧化亚铁硫杆菌能利用空气中的氧气将黄铁矿(主要成分为FeS2)氧化为Fe2(SO4)3,并使溶液酸性增强,其过程如图: